解答题-实验探究题 适中0.65 引用4 组卷222
铁和铝及其化合物在日常生产生活中有着广泛的应用。
I.制备 晶体(实验装置如图所示)
晶体(实验装置如图所示)
氯化铁( )是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下:
)是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下:___________ 。
(2)实验装置接口的连接顺序是a→___________ →g,G中盛装的物质是___________ ,其作用是___________ 。
(3)实验开始应先点燃___________ (填“A”或“B”)处的酒精灯,当观察到___________ 时(填现象),再点燃另一处的酒精灯。
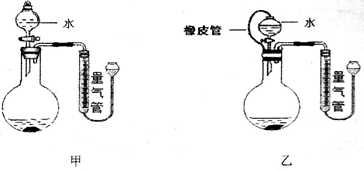
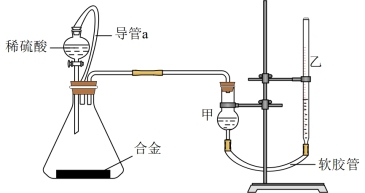
Ⅱ.测定铁铝合金中铝的质量分数(实验装置如图所示)___________ 。
(5)装置中导管a的作用除了使分液漏斗中的稀硫酸能顺利滴下以外,另一个作用是_______ 。
(6)若实验用铁铝合金的质量为0.334g,测得气体体积为67.2mL(已转换成标准状况),则合金中铝的质量分数为___________ (结果保留三位有效数字),该测量结果偏低,可能的原因是___________ (填字母)。
A.反应结束,未恢复至室温就读数
B.反应后读数时,甲侧液面低于乙侧液面
C.反应产生的气体没有完全被排入量气装置
D.反应后仰视刻度线读数
I.制备
氯化铁(
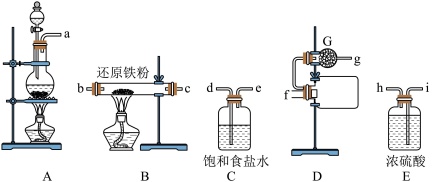
(2)实验装置接口的连接顺序是a→
(3)实验开始应先点燃
Ⅱ.测定铁铝合金中铝的质量分数(实验装置如图所示)
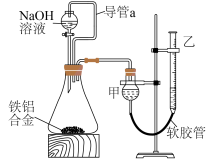
(5)装置中导管a的作用除了使分液漏斗中的稀硫酸能顺利滴下以外,另一个作用是
(6)若实验用铁铝合金的质量为0.334g,测得气体体积为67.2mL(已转换成标准状况),则合金中铝的质量分数为
A.反应结束,未恢复至室温就读数
B.反应后读数时,甲侧液面低于乙侧液面
C.反应产生的气体没有完全被排入量气装置
D.反应后仰视刻度线读数
23-24高一上·辽宁·阶段练习
类题推荐
氮化镁(Mg3N2)是一种重要的化学试剂。某化学兴趣小组拟制备氮化镁并测定产品纯度。
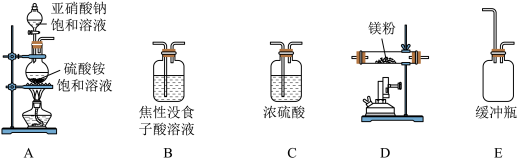
已知:①氮化镁极易与水反应;②亚硝酸钠和硫酸铵制取氮气的反应剧烈放热,产生氮气的速度较快;③焦性没食子酸溶液用于吸收少量O2。
(1)氮化镁的电子式为_______ 。
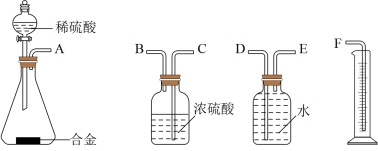
(2)结合信息,为制备氮化镁,图中实验装置(可重复使用)的连接顺序为A→_______ →_______ →_______ →_______ →_______ (按气流方向,用大写字母表示)。
(3)实验时在 D装置内加入镁粉,先点燃_______ (“A”或“D”)处酒精灯。
(4)定性分析
(5)定量测定
利用如图装置测定氮化镁产品纯度(杂质不产生气体,不考虑氨气在热水中的溶解)。
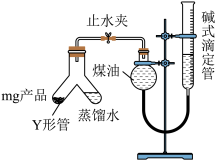
①当产品与蒸馏水完全反应后,_______ 、_______ 、调平液面、读数。
②取产品质量为 mg,开始滴定管读数为x1mL,最终滴定管读数为x2mL(折合成标准状况),则该样品纯度为_______ (用计算式表示)。如果开始仰视刻度线,终点时俯视刻度线,则测得结果_______ (填“偏高”“偏低”或“无影响”)。
已知:①氮化镁极易与水反应;②亚硝酸钠和硫酸铵制取氮气的反应剧烈放热,产生氮气的速度较快;③焦性没食子酸溶液用于吸收少量O2。

(1)氮化镁的电子式为
(2)结合信息,为制备氮化镁,图中实验装置(可重复使用)的连接顺序为A→
(3)实验时在 D装置内加入镁粉,先点燃
(4)定性分析
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量氮化镁样品于试管中,加足量蒸馏水 | 管底部有不溶物,试管变烫,产生有刺激性气味的气体 | ①写出反应的化学方程式 |
| 弃去上层清液,加入足量稀盐酸 | 观察到固体全部溶解且冒气泡 | ②冒气泡的原因是 |
利用如图装置测定氮化镁产品纯度(杂质不产生气体,不考虑氨气在热水中的溶解)。

①当产品与蒸馏水完全反应后,
②取产品质量为 mg,开始滴定管读数为x1mL,最终滴定管读数为x2mL(折合成标准状况),则该样品纯度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网