(1)Ti在元素周期表中的位置为
(2)试剂A为
(3)已知常温下,
(4)
(5)
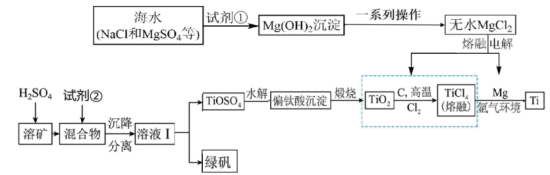
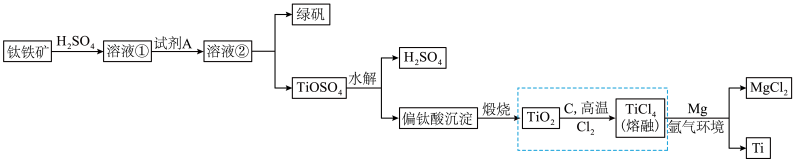
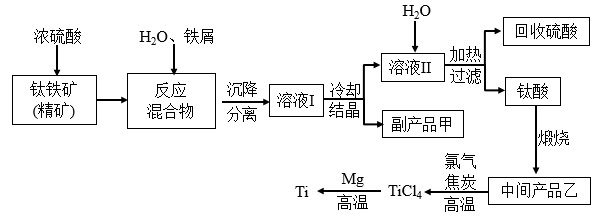
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下,回答下列问题:
(1)钛(Ti)在周期表中的位置:
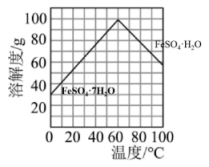
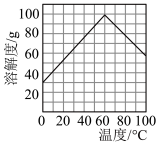
(2)钛铁矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成。副产品甲俗称“绿矾”其化学式是
(3)上述生产流程中加入Fe屑的目的是
(4)上述生产流程中所得到的金属钛中混有少量杂质,可加入
(5)溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
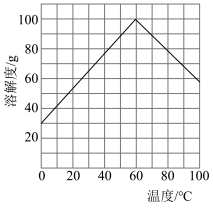
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当pH等于
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,写出该反应的离子方程式:
(6)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应控制的反应条件是
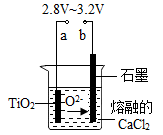
(7)在800--1000℃时电解TiO2也可制得海绵钛,装置如图所示。图中b是电源的
(1)下列状态的钛元素形成的微粒中,电离其最外层的一个电子所需能量最小的是_______(填序号)。
| A. | B. | C. | D. |
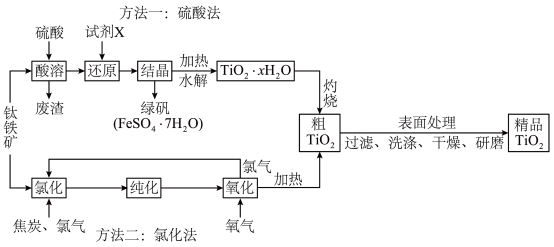
(2)“酸溶”时主要成分发生反应的离子方程式为
(3)“还原”时应选择合适的试剂X是
(5)以上两种工艺流程中,请说出方法一优于方法二的理由
(6)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网