解答题-原理综合题 较易0.85 引用2 组卷120
有以下多种物质,请回答相关问题:
①硫酸钠②氢氧化钡③醋酸④一水合氨⑤次氯酸钠⑦乙醇
(1)上述物质的水溶液显碱性的是___________ 。(填序号)
(2)从显碱性的溶液中任选一种,用化学用语说明其显碱性的原因___________ 。(写表达式)
(3)室温下,配制浓度均为0.1 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:某些弱酸在25℃时的电离常数如下:
①写出碳酸的第一级电离平衡常数 的计算公式
的计算公式___________ 。
②上述酸中酸性最强的是___________ 。(填化学式)
③25℃时,若次氯酸中初始 的物质的量浓度为0.01
的物质的量浓度为0.01 ,达到电离平衡时溶液中。
,达到电离平衡时溶液中。
___________ ( )
)
④下列反应可以发生的是___________ (填字母)。
A.
B.
C.
①硫酸钠②氢氧化钡③醋酸④一水合氨⑤次氯酸钠⑦乙醇
(1)上述物质的水溶液显碱性的是
(2)从显碱性的溶液中任选一种,用化学用语说明其显碱性的原因
(3)室温下,配制浓度均为0.1
①
资料:某些弱酸在25℃时的电离常数如下:
| 化学式 | |||||
| 电离常数 |
②上述酸中酸性最强的是
③25℃时,若次氯酸中初始
④下列反应可以发生的是
A.
B.
C.
23-24高二上·北京东城·期中
类题推荐
弱电解质在水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。①醋酸在水溶液中的电离方程式为_____ 。
②下列方法中,可以使醋酸溶液中 电离程度增大的是
电离程度增大的是_____ (填字母序号)。
a.滴加少量浓盐酸 b.加水稀释 c.加入少量醋酸钠晶体 d。升高温度
(2)某些弱酸在 时的电离常数如下:
时的电离常数如下:
①上述酸中酸性最强的是_____ 。
②下列反应可以发生的是_____ (填字母)。
A.
B.
C.
(3)测得 溶液显碱性,请用化学用语说明其显碱性的原因
溶液显碱性,请用化学用语说明其显碱性的原因_____ 。
(4)同浓度的 和
和 溶液的
溶液的 ,
,_____ 的 更大。
更大。
(1)醋酸是常见的弱酸。①醋酸在水溶液中的电离方程式为
②下列方法中,可以使醋酸溶液中
a.滴加少量浓盐酸 b.加水稀释 c.加入少量醋酸钠晶体 d。升高温度
(2)某些弱酸在
①上述酸中酸性最强的是
| 化学式 | |||||
| 电离常数 |
A.
B.
C.
(3)测得
(4)同浓度的
弱电解质在水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为_______ 。
②下列方法中,可以使醋酸溶液中 电离程度增大的是
电离程度增大的是_______ (填字母序号)。
a.滴加少量浓盐酸 b.加水稀释 c.加入少量醋酸钠晶体 d.升高温度
③两个密闭装置中各装入0.05g镁条,分别加入2mL2mol/L盐酸和醋酸。压强随时间变化如图所示。
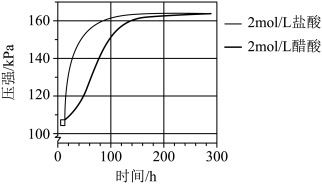
刚开始反应速率的关系是_______ 。原因是:_______ 。反应结束后两个容器中压强相等说明_______ 。
(2)某些弱酸在25℃时的电离常数如下:
①上述酸中酸性最强的是_______ 。
②25℃时,若次氯酸中初始HClO的物质的最浓度为0.01mol/L,达到电离平衡时溶液中
_______ mo/L。( )
)
③下列反应可以发生的是_______ (填字母)。
A.
B.
C.
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为
②下列方法中,可以使醋酸溶液中
a.滴加少量浓盐酸 b.加水稀释 c.加入少量醋酸钠晶体 d.升高温度
③两个密闭装置中各装入0.05g镁条,分别加入2mL2mol/L盐酸和醋酸。压强随时间变化如图所示。

刚开始反应速率的关系是
(2)某些弱酸在25℃时的电离常数如下:
| 化学式 | HSCN | HCN | HClO | ||
| 电离常数 |
②25℃时,若次氯酸中初始HClO的物质的最浓度为0.01mol/L,达到电离平衡时溶液中
③下列反应可以发生的是
A.
B.
C.
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
① 溶液和
溶液和 溶液中,
溶液中,
_____ 
②常温下,物质的量浓度相同的三种溶液:A. B.
B. C.
C. ,其pH由大到小的顺序是
,其pH由大到小的顺序是_____ (填编号)。
③将少量 通入
通入 溶液,反应的离子方程式是
溶液,反应的离子方程式是_____
④室温下,一定浓度的 溶液pH=9,用离子方程式表示溶液呈碱性的原因是
溶液pH=9,用离子方程式表示溶液呈碱性的原因是_____ ,溶液中
_____ (写出准确数值)
(2)某温度下,pH=3的盐酸中 该温度下,pH=2的
该温度下,pH=2的 与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为
与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为_____ 。
(3)室温下,用 盐酸溶液滴定
盐酸溶液滴定 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

d点所示的溶液中离子浓度由大到小的顺序依次为_____ 。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | |||
| 电离常数(25℃) |
②常温下,物质的量浓度相同的三种溶液:A.
③将少量
④室温下,一定浓度的
(2)某温度下,pH=3的盐酸中
(3)室温下,用

d点所示的溶液中离子浓度由大到小的顺序依次为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


