单选题 适中0.65 引用2 组卷139
实验室研究从炼铜烟灰(主要成分为CuO、Cu2O、ZnO、PbO及其硫酸盐)中分别回收铜、锌、铅元素的流程如下。
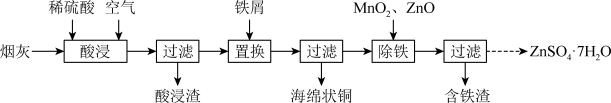
下列说法不正确 的是:

下列说法
| A.酸浸过程后,溶液中主要存在的离子有:Cu2+、Zn2+、Pb2+、H+、SO |
| B.铁屑加入初期,置换速率随时间延长而加快,其可能原因为:反应放热,温度升高,反应速率加快;Fe置换出的Cu,形成铁铜原电池,反应速率加快 |
| C.铁屑完全消耗后,铜的产率随时间延长而下降,其可能原因为生成的Fe2+被空气氧化为Fe3+,Fe3+与Cu反应,降低了Cu的产率 |
| D.海绵状铜中含有少量Fe、Zn、Pb,可通过精炼的方法提纯,海绵状铜连接外加电源正极 |
23-24高二上·江苏扬州·期中
类题推荐
实验室研究从炼铜烟灰(主要成分为CuO、Cu2O、ZnO、PbO及其硫酸盐)中分别回收铜、锌、铅元素的流程如下。
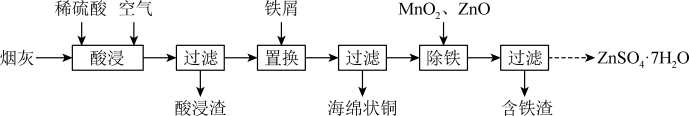
(1)酸浸过程中,金属元素均由氧化物转化为硫酸盐,其中生成CuSO4的化学方程式为:CuO + H2SO4 = CuSO4 + H2O、___________ 。
(2)铁屑加入初期,置换速率随时间延长而加快,其可能原因为:反应放热,温度升高;___________ 。铁屑完全消耗后,铜的产率随时间延长而下降,其可能原因为___________ 。
(3)已知:25 ℃时,Ksp(PbSO4)=2.5×10-8;PbSO4 + 2Cl- PbCl2 + SO
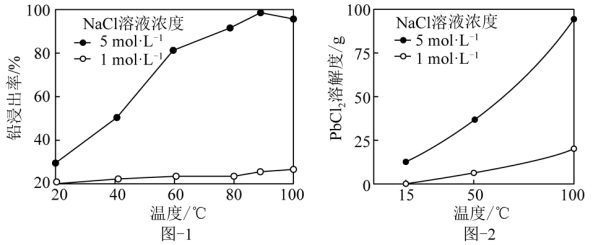
PbCl2 + SO 。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
浸出后溶液循环浸取并析出PbCl2的实验结果如下表所示。
①为提高原料NaCl溶液利用率,请补充完整利用酸浸渣制备化学纯(纯度≥98.5 %)PbCl2晶体的实验方案:取一定质量的酸浸渣,___________ ,将所得晶体洗涤、干燥。(可选用的试剂:5 mol·L-1NaCl溶液,1 mol·L-1NaCl溶液,NaCl固体)
②循环一定次数后的溶液中加入适量CaCl2溶液,过滤并加水稀释至其中NaCl浓度为1 mol·L-1的目的是___________ 。

(1)酸浸过程中,金属元素均由氧化物转化为硫酸盐,其中生成CuSO4的化学方程式为:CuO + H2SO4 = CuSO4 + H2O、
(2)铁屑加入初期,置换速率随时间延长而加快,其可能原因为:反应放热,温度升高;
(3)已知:25 ℃时,Ksp(PbSO4)=2.5×10-8;PbSO4 + 2Cl-

浸出后溶液循环浸取并析出PbCl2的实验结果如下表所示。
| 参数 | 循环次数 | |||
| 0 | 1 | 2 | 3 | |
| 结晶产品中PbCl2纯度/% | 99.9 | 99.3 | 98.7 | 94.3 |
②循环一定次数后的溶液中加入适量CaCl2溶液,过滤并加水稀释至其中NaCl浓度为1 mol·L-1的目的是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




