解答题-实验探究题 适中0.65 引用1 组卷16
回答下列问题:
【实验I】影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响。
药品: 、
、 、
、 和不同浓度的硫酸(0.5
和不同浓度的硫酸(0.5 、2
、2 、18.4
、18.4 );装置如图。
);装置如图。
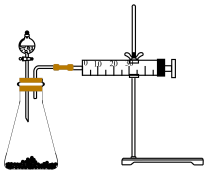
(1)实验前,检查该装置的气密性的方法是:___________ 。
(2)用此装置进行定量实验,应选用的上述实验药品是:
第一组:___________ 和___________ 。
第二组:___________ 和___________ 。
(3)应该测定的实验数据是气体从反应开始到推动活塞达到30 刻度时的
刻度时的___________ 。
(4)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):___________ 。
【实验II】已知反应:
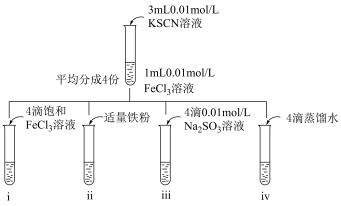
(5)i中现象为___________ 。
(6)ii中血红色褪去,结合离子反应和平衡移动解释原因___________ 。
(7)已知存在反应: ,设计实验iii和iv的目的是:
,设计实验iii和iv的目的是:___________ ,则证明iii中 影响平衡逆向移动的准确实验现象描述是
影响平衡逆向移动的准确实验现象描述是___________ 。
【实验I】影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响。
药品:

(1)实验前,检查该装置的气密性的方法是:
(2)用此装置进行定量实验,应选用的上述实验药品是:
第一组:
第二组:
(3)应该测定的实验数据是气体从反应开始到推动活塞达到30
(4)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):
【实验II】已知反应:

(5)i中现象为
(6)ii中血红色褪去,结合离子反应和平衡移动解释原因
(7)已知存在反应:
23-24高二上·广东茂名·阶段练习
类题推荐
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L)。设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表
(1)甲同学表中实验步骤②为____________________
(2)甲同学的实验目的是:在相同的温度下,__________________________________ 。
实验二:乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。
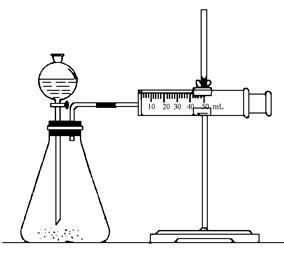
(3)乙同学在实验中应该测定的数据是______________ 。
(4)乙同学完成该实验应选用的实验药品是______________________ ;该实验中不选用某浓度的硫酸,理由是_________________________ 。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L)。设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol/L的硫酸于试管中② | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
(2)甲同学的实验目的是:在相同的温度下,
实验二:乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
根据下列实验设计,回答问题:
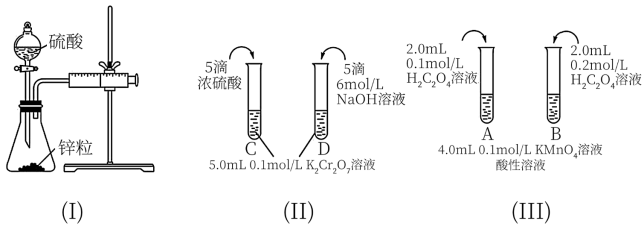
(1)利用实验(Ⅰ)探究锌与0.1 硫酸和2
硫酸和2 硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:
硫酸反应的速率,可以测定收集一定体积氢气所用的时间。检查该装置气密性的操作是:___________ 。
(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知: (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为___________ ,用平衡移动原理解释原因:___________ 。
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为___________ ,推测该实验设计能否达到实验目的并描述判断理由:___________ 。
(4)某小组也用酸性KMnO4溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:
①实验i、实验ii可得出的结论是___________ 。
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。
对反应有催化作用。利用提供的试剂设计实验iii,验证猜想。
提供试剂:0.01 酸性
酸性 溶液,0.1
溶液,0.1 草酸溶液,3
草酸溶液,3 硫酸,
硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。
补全实验iii的操作:向试管中先加入5 0.01
0.01 酸性
酸性 溶液,
溶液,___________ ,最后加入5 0.1
0.1 草酸溶液。
草酸溶液。

(1)利用实验(Ⅰ)探究锌与0.1
(2)实验(Ⅱ)探究浓度对化学化学平衡的影响。
已知:
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中反应离子方程式为
(4)某小组也用酸性KMnO4溶液和草酸(
| 编号 | 实验操作 | 实验现象 |
| i | 向一支试管中先加入5 | 前10 |
| ii | 向另一支试管中先加入5 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
提供试剂:0.01
补全实验iii的操作:向试管中先加入5
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



