填空题 适中0.65 引用2 组卷152
合成氨工艺是人工固氮最重要的途径。回答下列问题:
(1)工业合成氨的反应为 。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
①该反应的平衡常数表达式
_____ 。
②达到平衡时,H2的转化率为_____ 。
③在tmin内以NH3的浓度变化表示的化学反应速率为_____ 。
④若把容器的容积缩小一半,则正反应速率_____ (填“增大”、“减小”或“不变”,下同),N2的转化率_____ 。
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。铜氨液吸收CO适宜的生产条件是
。铜氨液吸收CO适宜的生产条件是_____ 。
(3)合成氨工业中采用循环操作,主要是为了_____ (填序号)。
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为
 ,该反应自发的条件是
,该反应自发的条件是_____ (填“低温自发”、“高温自发”或“任意温度自发”)。
②为提高CH4的平衡转化率,可采用的措施是_____ (填序号)。
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
(1)工业合成氨的反应为
①该反应的平衡常数表达式
②达到平衡时,H2的转化率为
③在tmin内以NH3的浓度变化表示的化学反应速率为
④若把容器的容积缩小一半,则正反应速率
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
(3)合成氨工业中采用循环操作,主要是为了
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为
②为提高CH4的平衡转化率,可采用的措施是
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
23-24高二上·天津南开·期中
类题推荐
合成氨技术的创立开辟了人工固氮的重要途径,其原理为:
 。请回答下列问题:
。请回答下列问题:
(1)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,其气体总物质的量随时间变化如下表:
则从反应开始到25min时,以H2表示的平均反应速率=___________ 。
(2)合成氨反应 ,初始时氮气、氢气的体积比为1:3,在相同催化剂条件下平衡混合物中氨的体积分数
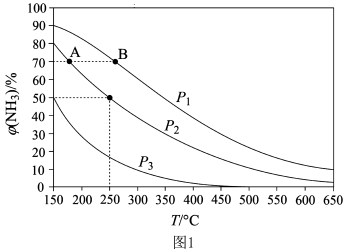
,初始时氮气、氢气的体积比为1:3,在相同催化剂条件下平衡混合物中氨的体积分数 与温度、压强的关系如图1所示。p1、p2、p3由大到小排序
与温度、压强的关系如图1所示。p1、p2、p3由大到小排序___________ ; A、B两点的化学反应速率较大的是___________ (填“A点”或“B点”)。
(3)在合成氨工业中,要使氨的平衡产率增大,同时又能提高反应速率,可采取的措施有___________ (填编号)。
①使用催化剂
②恒温恒容,增大原料气N2和H2充入量
③升高温度④恒温恒容,充入惰性气体Ar使压强增大
(4)工业上可以利用氨气生产氢氰酸(HCN)的反应为:
 ,在其他条件一定,该反应达到平衡时NH3转化率随外界条件Y变化的关系如图2所示,Y代表
,在其他条件一定,该反应达到平衡时NH3转化率随外界条件Y变化的关系如图2所示,Y代表___________ (填字母代号)。
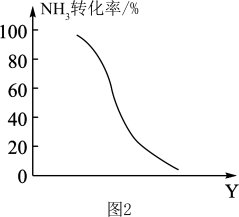
A.原料中CH4与NH3的体积比 B.温度 C.压强
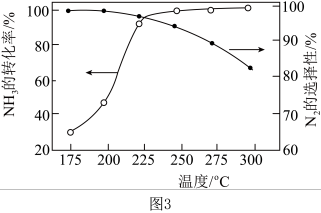
(5)NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去。将一定比例的NH3、O2和N2的混合气体以一定流速经过装有催化剂的反应管,NH3的转化率、N2的选择性 与温度的关系如图3。其他条件不变,在175~300℃范围内升高温度,出口处氮氧化物的量
与温度的关系如图3。其他条件不变,在175~300℃范围内升高温度,出口处氮氧化物的量___________ (填“增大”或“减小”),NH3的平衡转化率___________ (填“增大”或“减小”)。
(1)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1molN2和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,其气体总物质的量随时间变化如下表:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 气体总物质的量/mol | 4 | 3.52 | 3.3 | 3.16 | 3.06 | 3 | 3 |
(2)合成氨反应

(3)在合成氨工业中,要使氨的平衡产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂
②恒温恒容,增大原料气N2和H2充入量
③升高温度④恒温恒容,充入惰性气体Ar使压强增大
(4)工业上可以利用氨气生产氢氰酸(HCN)的反应为:

A.原料中CH4与NH3的体积比 B.温度 C.压强
(5)NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去。将一定比例的NH3、O2和N2的混合气体以一定流速经过装有催化剂的反应管,NH3的转化率、N2的选择性

工业合成氨是人类科学技术的一项重大突破。回答下列问题:
(1)合成氨工业中采用循环操作,主要是为了________ (填选项字母)。
(2)在密闭容器中通入amolN2和6molH2,若在一定条件下反应达到平衡状态,容器中剩余cmolN2。
①达到平衡时,H2转化率为________ 。
②若把容器的体积扩大一倍,则正反应速率_______ (填“增大”、“减小”或“不变”,下同),逆反应速率________ ,H2的转化率_______ 。
(3)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。
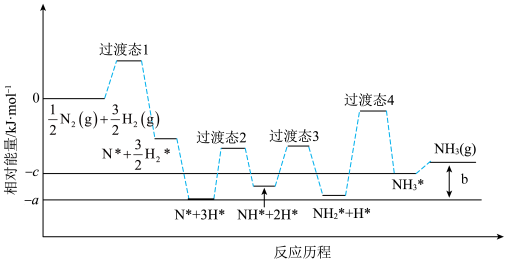
该反应历程中最大活化能对应步骤的化学方程式为_______ 。合成氨反应: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的△H=
NH3(g)的△H=_______ kJ/mol(用图中字母表示)。
(1)合成氨工业中采用循环操作,主要是为了
| A.增大化学反应速率 | B.提高氮气和氢气的利用率 |
| C.降低氨的沸点 | D.提高平衡混合物中氨的含量 |
(2)在密闭容器中通入amolN2和6molH2,若在一定条件下反应达到平衡状态,容器中剩余cmolN2。
①达到平衡时,H2转化率为
②若把容器的体积扩大一倍,则正反应速率
(3)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的微粒用*标注。

该反应历程中最大活化能对应步骤的化学方程式为
工业上合成氨工艺流程一般分三步:第一步为原料气的制备,将天然气等原料制成含氢和氮的粗原料气;第二步为净化,主要包括变换过程、脱硫脱碳过程以及气体精制过程;第三步为氨合成,将纯净的氢氮混合气压缩,增大压强,在催化剂的作用下合成氨。
(1)“一次转化”过程中 气体与水蒸气反应转化为CO和
气体与水蒸气反应转化为CO和 混合气体,已知几种物质的燃烧热如表所示:
混合气体,已知几种物质的燃烧热如表所示:
 的汽化热为
的汽化热为 ,则“一次转化”过程中生成CO的热化学方程式为
,则“一次转化”过程中生成CO的热化学方程式为______ 。
(2)“二步净化”过程中,原料 、
、 需要经过铜氨液处理净化,除去其中的CO,其反应为:
需要经过铜氨液处理净化,除去其中的CO,其反应为:
 ,铜氨液吸收CO适宜的生产条件是
,铜氨液吸收CO适宜的生产条件是______ (填字母)。
a.低温高压 b.高温高压 c.高温低压 d.低温低压
(3)第三步为氨合成,生产流程示意图如下。已知:

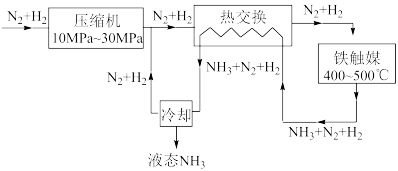
①上述流程中有利于提高原料利用率的措施有______ (请写出两点);
②有利于提高单位时间内氨的产率的措施有______ (请写出两点)。
(4)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,向1L密闭容器中充入1mol 和3mol
和3mol ,不同温度(
,不同温度( )、不同压强下,达平衡时混合物中
)、不同压强下,达平衡时混合物中 的物质的量分数的变化情况。
的物质的量分数的变化情况。
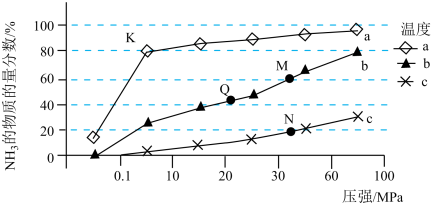
①曲线a对应的温度是______ ;
②M、N、Q点平衡常数的大小关系是______ ;K点的平衡常数为______ ;
③K点达平衡后再向容器中充入1mol 和2mol
和2mol ,平衡将
,平衡将______ (填“正向移动”、“逆向移动”或“不移动”)。
(1)“一次转化”过程中
物质 | ||||
燃烧热 | -285.5 | -890.3 | -283 | -393.5 |
(2)“二步净化”过程中,原料
a.低温高压 b.高温高压 c.高温低压 d.低温低压
(3)第三步为氨合成,生产流程示意图如下。已知:

①上述流程中有利于提高原料利用率的措施有
②有利于提高单位时间内氨的产率的措施有
(4)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,向1L密闭容器中充入1mol

①曲线a对应的温度是
②M、N、Q点平衡常数的大小关系是
③K点达平衡后再向容器中充入1mol
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


