解答题-原理综合题 较难0.4 引用1 组卷162
2022年3月4日,中国科学院大连化学物理研究所开发的全球首套1000吨/年二氧化碳加氢制汽油中试装置,在山东邹城工业园区开车成功,生产出符合国VI标准的清洁汽油,这有助于我国在2030年前实现碳达峰。回答下列问题:
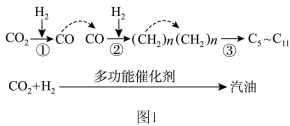
(1)CO2催化加氢制取汽油时,CO2的转化过程如图1:
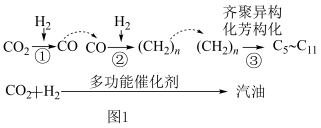
下列对该反应过程的说法正确的是________ (填标号)。
(2)写出反应①的化学方程式_______ 。
(3)如将CO2与H2以1:3的体积比混合。
①适当条件下合成某烃和水,该烃可能是______ (填序号)。
A.烷烃 B.烯烃 C.炔烃 D.苯的同系物
②适当条件下合成燃料甲醇和水。在恒温恒容的密闭容器中,充入2molCO2和6molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列能说明反应达到平衡状态的是
CH3OH(g)+H2O(g),下列能说明反应达到平衡状态的是______ (填字母)
A.混合气体密度保持不变
B.混合气体的平均相对分子质量不变
C.CO2和H2的体积比保持不变
D.断裂2mol碳氧双键的同时生成3molH-H键
(4)催化剂通过参与反应,改变反应的途径,降低反应活化能,加快化学反应速率,反应的热效应△H______ (填“减小”、“增大”或“不变”)。
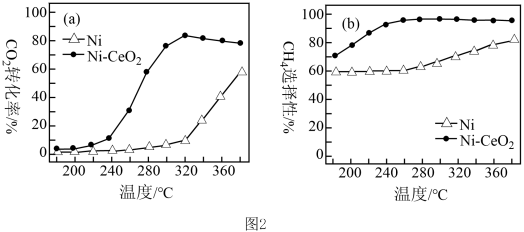
(5)已知CO2甲烷化技术的反应原理为CO2(g)+4H2(g) CH4(g)+2H2O(g) △H<0,该技术的核心是催化剂的选择。其他条件均相同,在两种不同催化剂条件下反应相同时间,测得CO2转化率和CH4选择性(选择性是指产生这个物质所消耗的反应物的量占总的反应物的量的比例大小)随温度变化的曲线如图2所示。
CH4(g)+2H2O(g) △H<0,该技术的核心是催化剂的选择。其他条件均相同,在两种不同催化剂条件下反应相同时间,测得CO2转化率和CH4选择性(选择性是指产生这个物质所消耗的反应物的量占总的反应物的量的比例大小)随温度变化的曲线如图2所示。
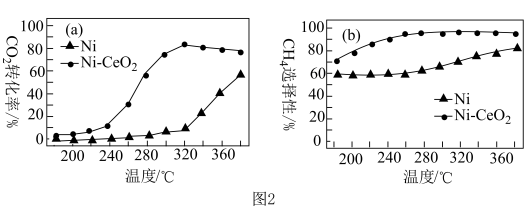
以Ni为催化剂,高于320℃后,单位时间内CO2转化率上升的原因是______ ,工业上应选择的催化剂是______ 。
(1)CO2催化加氢制取汽油时,CO2的转化过程如图1:

下列对该反应过程的说法正确的是
| A.整个反应过程中,有非极性键和极性键的断裂和形成 |
B.CO2的电子式为 ,为非极性分子 ,为非极性分子 |
| C.汽油为纯净物 |
| D.①②反应一定有水生成 |
(2)写出反应①的化学方程式
(3)如将CO2与H2以1:3的体积比混合。
①适当条件下合成某烃和水,该烃可能是
A.烷烃 B.烯烃 C.炔烃 D.苯的同系物
②适当条件下合成燃料甲醇和水。在恒温恒容的密闭容器中,充入2molCO2和6molH2,一定条件下发生反应:CO2(g)+3H2(g)
A.混合气体密度保持不变
B.混合气体的平均相对分子质量不变
C.CO2和H2的体积比保持不变
D.断裂2mol碳氧双键的同时生成3molH-H键
(4)催化剂通过参与反应,改变反应的途径,降低反应活化能,加快化学反应速率,反应的热效应△H
(5)已知CO2甲烷化技术的反应原理为CO2(g)+4H2(g)

以Ni为催化剂,高于320℃后,单位时间内CO2转化率上升的原因是
23-24高三上·四川广安·阶段练习
类题推荐
推进能源绿色转型,实现碳达峰、碳中和,事关经济社会发展全局。CO2甲烷化及甲烷重整制甲醇是能源综合利用领域的研究热点。回答下列问题:
(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+ O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H,反应的部分历程如图所示(吸附在催化剂表面的物种用“*”标注,TS代表过渡态)。下列说法正确的是_____ (填标号)。
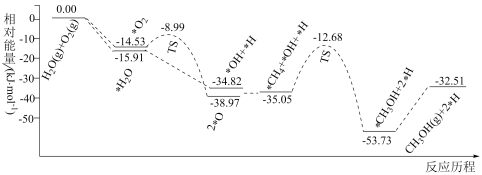
(2)催化剂的选择是CO2甲烷化的核心,金属Ni或Ni-CeO2均可作为催化剂。
①基态Ni原子的核外电子排布式为_____ 。
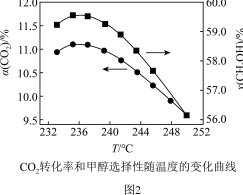
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是____ 。对比上述两种催化剂的催化性能,工业上应选择的催化剂和温度分别是____ 。
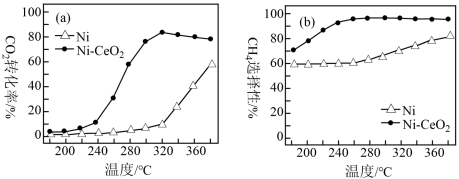
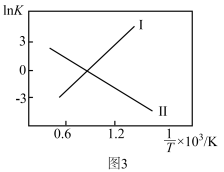
(3)一定条件下,发生反应CO(g)+3H2(g) CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m=
CH4(g)+H2O(g) △H=-198kJ•mol-1,测CO的平衡转化率与温度、起始投料比m[m= ]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。
]的关系如图所示。已知v正=k正•c(CO)•c3(H2),v逆=k逆•c(CH4)•c(H2O) (k正、k逆为速率常数,只与温度有关)。

①图中m1、m2、m3由大到小的顺序为_____ 。
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=____ mol•L-1•s-1。平衡时k正:k逆=____ ,达到平衡后,升高温度,k正:k逆_____ (填“增大”、“减小”或“不变”)。
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为____ 。

(1)已知CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面可合成甲醇:CH4(g)+

| A.该反应的△H=-32.5kJ•mol-1 |
| B.H2O(g)比O2(g)更容易吸附在催化剂表面 |
| C.该反应过程中只涉及σ键的断裂与形成 |
| D.图中慢反应的化学方程式为*CH4+*OH=*CH3OH+*H |
①基态Ni原子的核外电子排布式为
②在上述两种催化剂的条件下反应相同时间,测得CO2转化率和CH4选择性随温度的变化如图所示。高于320℃,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是

(3)一定条件下,发生反应CO(g)+3H2(g)

①图中m1、m2、m3由大到小的顺序为
②向一体积为2L的恒容密闭容器中充入1molCO和3molH2,在一定温度下,经5s达到平衡,此时CO的转化率为50%。0~5s内,v(H2)=
(4)微生物电化学产甲烷法的装置如图所示。b电极的电极反应式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网