解答题-工业流程题 适中0.65 引用1 组卷45
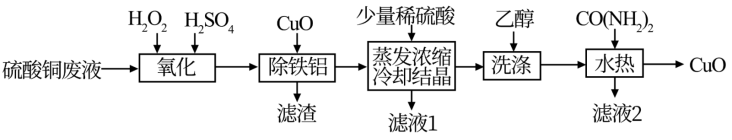
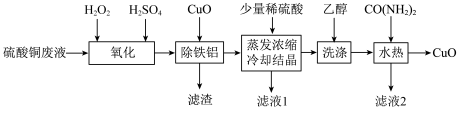
2021年6月24日,《一种硫酸铜废液制备高纯氧化铜》获得第22届中国专利优秀奖,其工艺流程如图:
已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
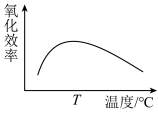
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式________ ;如图是双氧水的氧化效率随温度变化的曲线,请解释氧化效率变化的原因________ 。
(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至______ (lg2=0.3)。
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为______ ,洗涤所需要的玻璃仪器有______ ,判断晶体洗涤干净的实验操作是________ 。
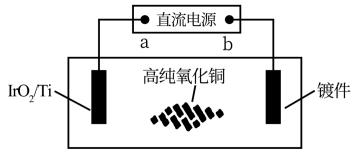
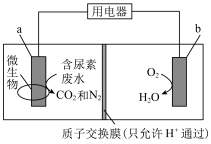
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是________ 。

已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式

(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是

| A.温度越高,反应速率越快,装置的转化率越高 |
| B.该装置工作时,b为正极,发生还原反应 |
| C.装置内溶液电流的方向由 |
| D.工作一段时间后,正极区域pH会显著升高 |
23-24高三上·四川广安·阶段练习
类题推荐
锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为 ,还含有铁、钴、镍、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
,还含有铁、钴、镍、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
表一
表二
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有_______ (写两种)。
(2)“氧化”步骤发生反应的离子方程式为_______ 。
(3)滤渣1的主要成分是_______ ,实验室中为了加快固液混合物的分离,常采用的操作是_______ 。
(4)有同学提出,加入(NH4)2S除钴、除镍的步骤可以放在“除杂1”之前,你是否赞同?请说明理由:_______ 。
(5)由 晶体制备CuCl2的方法是
晶体制备CuCl2的方法是_______ 。
(6)25℃时,分离出滤渣3所得的滤液中 =
=_______ ,欲使沉钴后的溶液中 ,需要控制溶液的pH至少为
,需要控制溶液的pH至少为_______ 。(已知
(7)电解废液中还含有少量Mn2+,向其中加入饱和N 溶液,有沉淀和气体生成,该反应的离子方程式为
溶液,有沉淀和气体生成,该反应的离子方程式为_______ 。

表一
| 物质 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp |
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有
(2)“氧化”步骤发生反应的离子方程式为
(3)滤渣1的主要成分是
(4)有同学提出,加入(NH4)2S除钴、除镍的步骤可以放在“除杂1”之前,你是否赞同?请说明理由:
(5)由
(6)25℃时,分离出滤渣3所得的滤液中
(7)电解废液中还含有少量Mn2+,向其中加入饱和N
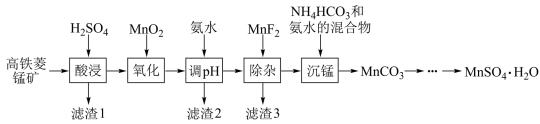
一水硫酸锰(MnSO4•H2O)是一种重要的化工中间体,工业上可由高铁菱锰矿(主要成分为MnCO3,含有FeCO3、Al2O3、MgO、CaO、SiO2等杂质)制备,部分工艺流程如下:
相关金属离子[c(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的 pH范围如下:
(1)“酸浸”时高铁菱锰矿需要粉碎,并进行充分搅拌,为提高锰的浸出率还可采取的措施有_________ 。(写出其中一种)
(2)“氧化”时发生反应的化学方程式为________ 。
(3)“调pH”范围至5~6,得到滤渣2的主要成分除MnO2外还有_________ 。
(4)“除杂”过程中加入MnF2的目的是_________ 。已知:Ksp(MgF2)=5.16×10-11,Ksp(CaF2)=5.3×10-9。
(5)“沉锰”过程中发生反应的离子方程式为_________ 。
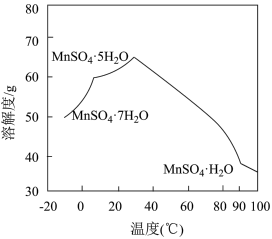
(6)MnSO4在水中的溶解度与温度关系如图。由MnCO3获得较纯净的MnSO4•H2O 晶体的方法是:将MnCO3溶于_________ ,控制温度为_________ 以上结晶,得到MnSO4•H2O晶体,洗涤、烘干。晶体烘干时温度不能过高的原因是_________ 。

相关金属离子[c(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的 pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(2)“氧化”时发生反应的化学方程式为
(3)“调pH”范围至5~6,得到滤渣2的主要成分除MnO2外还有
(4)“除杂”过程中加入MnF2的目的是
(5)“沉锰”过程中发生反应的离子方程式为
(6)MnSO4在水中的溶解度与温度关系如图。由MnCO3获得较纯净的MnSO4•H2O 晶体的方法是:将MnCO3溶于

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网