解答题-实验探究题 较难0.4 引用4 组卷473
某小组用淀粉水解液和浓 (作催化剂)、
(作催化剂)、 为原料制取草酸晶体(
为原料制取草酸晶体( ),进而制备纳米草酸钙(
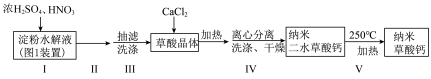
),进而制备纳米草酸钙( ),按如下流程开展实验(夹持仪器略):
),按如下流程开展实验(夹持仪器略):
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式: 。
。
(1)仪器甲相比普通分液漏斗的优点是___________ ,仪器乙的名称为___________ ,步骤Ⅱ的操作名称是___________ 。
(2) 不与
不与 反应,但在本实验中可以完全被吸收,请用离子方程式表示
反应,但在本实验中可以完全被吸收,请用离子方程式表示 被完全吸收的原因
被完全吸收的原因___________ 。
(3)催化剂浓硫酸用量过多,会导致草酸产率减少,原因是___________ 。
(4)下列有关操作说法正确的是___________。
(5)草酸晶体( )含有结晶水,某同学准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用
)含有结晶水,某同学准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用 标准溶液滴定,若草酸晶体中混有
标准溶液滴定,若草酸晶体中混有 ,则该滴定法测得产品中x的值
,则该滴定法测得产品中x的值___________ (填“偏大”“偏小”、“无影响”)。
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式:
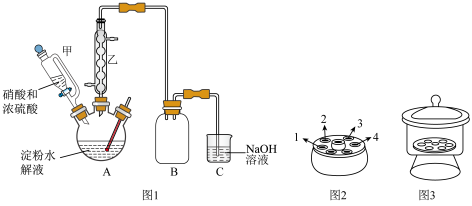
(1)仪器甲相比普通分液漏斗的优点是
(2)
(3)催化剂浓硫酸用量过多,会导致草酸产率减少,原因是
(4)下列有关操作说法正确的是___________。
| A.步骤Ⅲ洗涤可用乙醇水溶液,步骤Ⅳ洗涤可用蒸馏水 |
| B.步骤Ⅳ采用离心分离,装置如图2所示,操作时应将两支离心管放置于1、4处 |
| C.步骤Ⅳ干燥采用图3装置,取用时,手握干燥器盖顶圆球向上拉,取下盖子倒放在桌上,将装有产品的器皿放在陶瓷板上 |
| D.步骤Ⅴ为提高反应速率,也可采用更高温度加热 |
(5)草酸晶体(
23-24高三上·山东济宁·期中
类题推荐
某兴趣小组用淀粉水解液和浓 为原料制取草酸晶体
为原料制取草酸晶体 ,进而制备纳米草酸钙
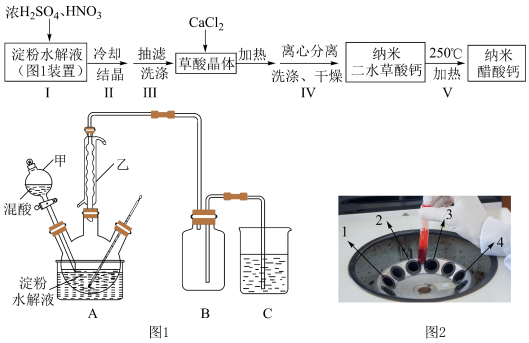
,进而制备纳米草酸钙 ,按如下流程开展了实验(夹持仪器已省略):
,按如下流程开展了实验(夹持仪器已省略):
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式: (
( 作催化剂)。
作催化剂)。
请回答:
(1)图1装置中仪器乙的名称___________ 。若C烧杯中盛放足量氢氧化钠溶液,写出C中发生反应的离子方程式___________ (假设气体全部被吸收),除了氢氧化钠溶液,还可以选用___________ (至少写出两种溶液)。
(2)下列有关操作说法不正确 的是___________。
(3)步骤Ⅳ中离心分离后得到的滤液中加入氨水还会析出产品沉淀,请结合离子方程式和平衡移动原理加以解释___________ 。
(4)草酸晶体 含有结晶水,某同学通过如下实验测定其组成:
含有结晶水,某同学通过如下实验测定其组成:
①配制标准氢氧化钠溶液:称取一定质量氢氧化钠固体,用适量水溶解后,选择合适的操作并排序(步骤可重复使用),配制溶液:___________
a→b→(___________)→(___________)→f→d→(___________)→(___________)→h
a.检查容量瓶玻璃塞处是否漏水b.将烧杯中的液体全部转移到容量瓶中
c.用蒸馏水洗涤烧杯和玻璃棒2-3次d.加蒸馏水至容量瓶接近标线
e.盖好瓶塞,反复上下颠倒容量瓶f.轻轻摇动容量瓶
g.离刻度线 时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签
时,改用胶头滴管加水至凹液面与刻度线相切h.装瓶贴标签
②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述 标准溶液滴定。若草酸晶体中混有
标准溶液滴定。若草酸晶体中混有 ,则该滴定法测得产品中
,则该滴定法测得产品中 的值
的值___________ (填“偏大”“偏小”“无影响”)。
②纳米草酸钙难溶于水,高温易分解;
③淀粉水解液与混酸反应的方程式:
请回答:
(1)图1装置中仪器乙的名称
(2)下列有关操作说法
| A.步骤Ⅱ采取冷却结晶,以防止草酸晶体失水 |
| B.步骤Ⅲ洗涤可用乙醇水溶液,步骤IV洗涤可用蒸馏水洗涤 |
| C.步骤Ⅴ采用 |
| D.步骤Ⅳ采用离心分离,装置如图2所示,操作时应将两支离心管放置于1、4处 |
(3)步骤Ⅳ中离心分离后得到的滤液中加入氨水还会析出产品沉淀,请结合离子方程式和平衡移动原理加以解释
(4)草酸晶体
①配制标准氢氧化钠溶液:称取一定质量氢氧化钠固体,用适量水溶解后,选择合适的操作并排序(步骤可重复使用),配制溶液:
a→b→(___________)→(___________)→f→d→(___________)→(___________)→h
a.检查容量瓶玻璃塞处是否漏水b.将烧杯中的液体全部转移到容量瓶中
c.用蒸馏水洗涤烧杯和玻璃棒2-3次d.加蒸馏水至容量瓶接近标线
e.盖好瓶塞,反复上下颠倒容量瓶f.轻轻摇动容量瓶
g.离刻度线
②标定氢氧化钠溶液的浓度。
③滴定:准确称取一定质量草酸晶体于锥形瓶中,用蒸馏水溶解,以酚酞作指示剂,用上述
某兴趣小组用二氧化锰(MnO2)和草酸晶体(H2C2O4•2H2O)为原料制备碳酸锰(MnCO3),按如图流程开展了实验: 
已知:①碳酸锰几乎不溶于水,不溶于醇,溶于稀无机酸;受热易分解。
②Mn(Ⅳ)在酸性条件下易被还原为Mn(Ⅱ),Mn(Ⅱ)在碱性条件下易被氧化为Mn(Ⅳ)。
请回答:
(1)加入稀硫酸的作用是____ 。
(2)步骤Ⅰ:反应的离子方程式是____ 。
(3)下列操作中正确的是____ 。
(4)步骤Ⅳ抽滤、洗涤操作可用如图装置进行,打开活塞K,打开抽气泵,转移固液混合物,关闭活塞K,确认抽干,进行洗涤。请给出洗涤的操作排序(洗涤操作只需考虑一次):a→c→(____)→(____)→(____)→(____)→将产品转至干燥器。____
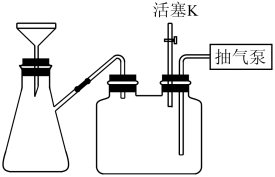
a.打开活塞K b.关闭活塞K c.加洗涤剂洗涤 d.打开抽气泵 e.关闭抽气泵 f.确认抽干
(5)用吸光光度法确定MnCO3产品纯度:通过对比样品溶液与标准溶液的吸光度测产品的纯度。准确称取Wg产品,用稀硝酸溶解,加入足量过二硫酸铵溶液作氧化剂,以硝酸银作催化剂,加热,反应方程式如下:
MnCO3+2HNO3=Mn(NO3)2+CO2↑+H2O
Mn(NO3)2+5(NH4)2S2O8+8H2O=2HMnO4+5(NH4)2SO4+5H2SO4+4HNO3
反应结束用蒸馏水定容至100mL,取10mL至比色管中,测得溶液中MnO 的吸光度为A,A=kc(k为常数,c为浓度),则MnCO3产品纯度是
的吸光度为A,A=kc(k为常数,c为浓度),则MnCO3产品纯度是____ (用含W、A、k的式子表示)。取待测液于比色管中时,移液管未润洗,测得产品纯度将____ (填“偏高”或“偏低”或“无影响”)。

已知:①碳酸锰几乎不溶于水,不溶于醇,溶于稀无机酸;受热易分解。
②Mn(Ⅳ)在酸性条件下易被还原为Mn(Ⅱ),Mn(Ⅱ)在碱性条件下易被氧化为Mn(Ⅳ)。
请回答:
(1)加入稀硫酸的作用是
(2)步骤Ⅰ:反应的离子方程式是
(3)下列操作中正确的是
| A.步骤Ⅱ将滤纸放入布氏漏斗内,用蒸馏水润湿滤纸 |
| B.步骤Ⅳ不宜烘干,可以选用减压干燥 |
| C.边搅拌边缓慢滴加饱和碳酸氢铵溶液,避免局部碱性过大使Mn(II)氧化 |
| D.步骤Ⅳ用乙醇作为洗涤剂,洗涤结束后,将固体迅速转移并进行后续操作 |

a.打开活塞K b.关闭活塞K c.加洗涤剂洗涤 d.打开抽气泵 e.关闭抽气泵 f.确认抽干
(5)用吸光光度法确定MnCO3产品纯度:通过对比样品溶液与标准溶液的吸光度测产品的纯度。准确称取Wg产品,用稀硝酸溶解,加入足量过二硫酸铵溶液作氧化剂,以硝酸银作催化剂,加热,反应方程式如下:
MnCO3+2HNO3=Mn(NO3)2+CO2↑+H2O
Mn(NO3)2+5(NH4)2S2O8+8H2O=2HMnO4+5(NH4)2SO4+5H2SO4+4HNO3
反应结束用蒸馏水定容至100mL,取10mL至比色管中,测得溶液中MnO
硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备 。
。

合成反应: 、
、 、
、
滴定反应: 。
。
已知: 易溶于水,难溶于乙醇,50℃开始失结晶水。
易溶于水,难溶于乙醇,50℃开始失结晶水。
实验步骤:
Ⅰ. 制备:
制备:
装置A制备的 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液pH约为7时,停止通入
经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液pH约为7时,停止通入 气体,得产品混合溶液。
气体,得产品混合溶液。
Ⅱ.产品分离提纯:
产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到 产品。
产品。
Ⅲ.产品纯度测定:
以淀粉作指示剂,取ag 产品配制成200mL溶液,滴定20.00mL浓度为bmol/L的碘标准溶液至终点,用去
产品配制成200mL溶液,滴定20.00mL浓度为bmol/L的碘标准溶液至终点,用去 溶液cmL,计算
溶液cmL,计算 含量。请回答:
含量。请回答:
(1)装浓 的仪器名称为
的仪器名称为___________ ;步骤I:单向阀的作用是___________ ;装置C中的反应混合溶液pH过高或过低将导致产率降低,原因是___________ 。
(2)步骤Ⅱ:下列说法正确的是___________。
(3)步骤Ⅲ
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):___________ 。
检漏→蒸馏水洗涤→ → → → → →开始滴定。
A.烘干 B.记录起始读数 C.调整滴定液液面至零刻度或零刻度以下 D.排除气泡
E.用洗耳球吹出润洗液 F.用滴定液润洗2至3次 G.装入滴定液至零刻度以上
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是________ 。
③试计算 的纯度为
的纯度为___________ (用含a、b、c的代数式表示)。若滴定法测得产品中 含量为100.5%,则
含量为100.5%,则 产品中可能混有的物质是
产品中可能混有的物质是___________ 。

合成反应:
滴定反应:
已知:
实验步骤:
Ⅰ.
装置A制备的
Ⅱ.产品分离提纯:
产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
Ⅲ.产品纯度测定:
以淀粉作指示剂,取ag
(1)装浓
(2)步骤Ⅱ:下列说法正确的是___________。
| A.快速蒸发溶液中水分,可得较大晶体颗粒 |
| B.蒸发浓缩至溶液表面出现品晶膜时,停止加热 |
| C.冷却结晶后的固液混合物中加入乙醇可提高产率 |
| D.可选用冷的 |
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→ → → → → →开始滴定。
A.烘干 B.记录起始读数 C.调整滴定液液面至零刻度或零刻度以下 D.排除气泡
E.用洗耳球吹出润洗液 F.用滴定液润洗2至3次 G.装入滴定液至零刻度以上
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是
③试计算
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


