解答题-原理综合题 较易0.85 引用1 组卷15
回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应: 。已知该反应为放热反应,如图能正确表示该反应中能量变化的是
。已知该反应为放热反应,如图能正确表示该反应中能量变化的是______ 。
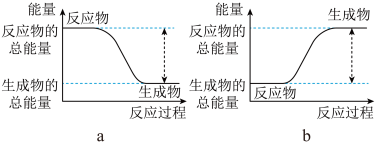
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
反应 的
的
______ kJ/mol。则该反应生成1 mol  可以放出热量是
可以放出热量是______ kJ。
(2) 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生 ,若将此反应设计成原电池,则负极所用电极材料为:
,若将此反应设计成原电池,则负极所用电极材料为:______ 。当线路中转移0.2 mol电子时,则被腐蚀铜的质量为:______ g。
(3)铅蓄电池在放电时发生的电池反应式为: ,负极电极反应式为:
,负极电极反应式为:__________________ 。
(1)从能量的变化和反应的快慢等角度研究反应:

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
| 化学键 | |||
| 键能(kJ/mol) | 436 | 496 | 463 |
(2)
(3)铅蓄电池在放电时发生的电池反应式为:
23-24高二上·海南海口·阶段练习
类题推荐
在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
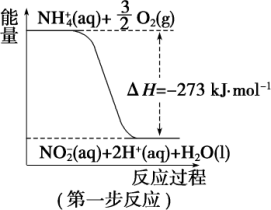
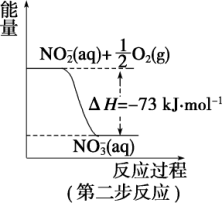
(1)第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
(2)1 molNH (aq) 全部氧化成NO
(aq) 全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:
该反应的热化学方程式是_______ 。
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为_______ ;电解质溶液为_______ ,当电路中转移0.2 mol 电子时,被腐蚀的负极反应物的质量为_______ g。


(1)第一步反应是
(2)1 molNH
(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2
| 化学键 | H-Cl | O=O | Cl-Cl | H-O |
| 键能/kJ/mol | 431 | 498 | 243 | 463 |
该反应的热化学方程式是
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为
从能量的变化和反应的快慢等角度研究反应具有重要意义。
(1)已知反应2H2(g)+O2(g)=2H2O(g)为放热反应,下图能正确表示该反应中能量变化的是_______ 。
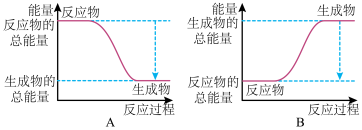
从断键和成键的角度分析上述反应中能量的变化。化学键的键能如上表:则生成1mol液态水可以放出热量____________ kJ
(2)将质量相同的铜棒和锌棒用导线连接后插入CuSO4溶液中,设计成原电池,负极材料是______________ , 正极的反应式为______________ ,电解质溶液中SO42- 移向______ 极(填“正”或“负”)。
(3)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为______ ;X为______ 。若反应经2min时C的浓度______ 0.8mol/L(填“大于,小于或等于”)。
(1)已知反应2H2(g)+O2(g)=2H2O(g)为放热反应,下图能正确表示该反应中能量变化的是

| 化学键 | H—H | O=O | H—O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)将质量相同的铜棒和锌棒用导线连接后插入CuSO4溶液中,设计成原电池,负极材料是
(3)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)
回答下列问题。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。
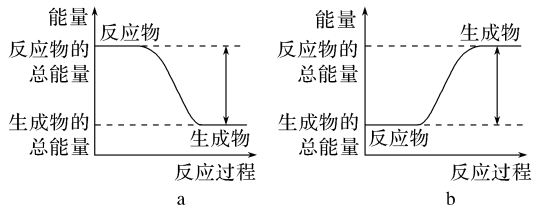
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
反应2H2(g)+O2(g)=2H2O(g)的ΔH=_______ kJ/mol。生成1 mol H2O(g)可以放出热量是_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
| 化学键 | H—H | O=O | H—O |
| 键能(kJ/mol) | 436 | 496 | 463 |
反应2H2(g)+O2(g)=2H2O(g)的ΔH=
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


