解答题-实验探究题 较难0.4 引用1 组卷158
草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体(H2C2O4·2H2O),并验证其具有的某些性质。回答下列问题:
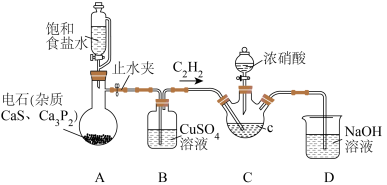
(1)仪器C的名称是_________ 。有人经分析后认为,用质量分数为70%的酒精溶液代替饱和食盐水(20℃时NaCl溶解度为36g)可获得更为平稳的气流,他得出这种结论的依据是_______ 。
(2)装置B的作用是_______________ ,若实验中使用上述酒精溶液代替食盐水,并且利用酸性KMnO4溶液检验有乙炔生成,则气体通过B后应先通入到盛有__________ 的洗气瓶,最后通入到酸性KMnO4溶液中。
(3)草酸在装置C中生成,反应的化学方程式为__________ ,装置D的作用是___________ 。
(4)待反应结束后,从C中分离出草酸晶体,然后用0.1000mol/L的酸性KMnO4溶液进行滴定以测定其纯度。
①称量3.500g草酸晶体配制100mL溶液,下 列配制操作中错误的是________ (填标号)。
a. b.
b. c.
c. d.
d. 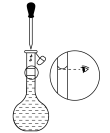
②三次平行滴定实验中消耗KMnO4溶液的体积如下表所示,其中第一次实验滴定后的液面位置如图所示。
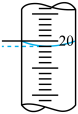
则V=_____ mL,样品中草酸晶体的质量分数为___________ 。

(1)仪器C的名称是
(2)装置B的作用是
(3)草酸在装置C中生成,反应的化学方程式为
(4)待反应结束后,从C中分离出草酸晶体,然后用0.1000mol/L的酸性KMnO4溶液进行滴定以测定其纯度。
①称量3.500g草酸晶体配制100mL溶液,下 列配制操作中错误的是
a.
 b.
b. c.
c. d.
d. 
②三次平行滴定实验中消耗KMnO4溶液的体积如下表所示,其中第一次实验滴定后的液面位置如图所示。

| 滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积/mL | ||
| 第一次 | 20.00 | 0.20 | V1 | |
| 第二次 | 20.00 | 2.56 | 23.40 | |
| 第三次 | 20.00 | 0.22 | 20.32 | |
23-24高三上·内蒙古鄂尔多斯·阶段练习
类题推荐
草酸(H2C2O4)是一种常见二元弱酸,易溶于水,常用来做还原剂、沉淀剂、媒染剂、络合剂等。某化学学习兴趣小组欲制备草酸并探究其某些化学性质,经查找资料:乙炔在45-55℃硝酸汞作催化剂的条件下,经浓硝酸氧化可制得草酸。
[草酸的制备]
甲同学以电石(主要成分CaC2)、浓硝酸及少量硝酸汞为原料,利用如图装置制备草酸。

(1)仪器a的名称_______
(2)实验室制乙炔时用饱和食盐水代替水的目的是。_______ 。反应时C中产生大量红棕色气体,请写出C中发生化学反应方程式_______ 。
[产品中草酸晶体(H2C2O4·2H2O)质量分数的测定]
乙同学准确称取ag产品,配成100mL水溶液,取20mL所配制的溶液置于锥形瓶内,用cmol·L-1酸性KMnO4标准溶液滴定至终点,平行实验三次,平均消耗标准溶液vmL。试回答:
(3)上述滴定实验中发生的离子反应方程式_______ ,判断到达滴定终点的现象是_______ 。
(4)产品中草酸晶体(H2C2O4·2H2O)的质量分数为_______ (用a、v表示)
[草酸的性质]
(5)上述酸性高锰酸钾与草酸反应,体现了草酸_______ (填酸性、氧化性或还原性)
(6)室温下已知:Ka1(H2C2O4)=5.6×10-2,Ka2(H2C2O4)=1.5×104,通过下列实验探究草酸的性质。[1g2=0.3,lg3=0.5]。向10mL0.1mol/LH2C2O4溶液中逐滴加入VmL0.1mol/LNaOH溶液,当V从0逐渐增大至20时,测得混合溶液的pH逐渐增大,下列说法正确的是_______(填字母)
[草酸的制备]
甲同学以电石(主要成分CaC2)、浓硝酸及少量硝酸汞为原料,利用如图装置制备草酸。

(1)仪器a的名称
(2)实验室制乙炔时用饱和食盐水代替水的目的是。
[产品中草酸晶体(H2C2O4·2H2O)质量分数的测定]
乙同学准确称取ag产品,配成100mL水溶液,取20mL所配制的溶液置于锥形瓶内,用cmol·L-1酸性KMnO4标准溶液滴定至终点,平行实验三次,平均消耗标准溶液vmL。试回答:
(3)上述滴定实验中发生的离子反应方程式
(4)产品中草酸晶体(H2C2O4·2H2O)的质量分数为
[草酸的性质]
(5)上述酸性高锰酸钾与草酸反应,体现了草酸
(6)室温下已知:Ka1(H2C2O4)=5.6×10-2,Ka2(H2C2O4)=1.5×104,通过下列实验探究草酸的性质。[1g2=0.3,lg3=0.5]。向10mL0.1mol/LH2C2O4溶液中逐滴加入VmL0.1mol/LNaOH溶液,当V从0逐渐增大至20时,测得混合溶液的pH逐渐增大,下列说法正确的是_______(填字母)
| A.当V=10时,溶液中离子浓度关系:c(Na+)>c(HC2O |
| B.当溶液中c(C2O |
| C.当溶液中c(C2O |
| D.当溶液中c(Na+)=2c(C2O |
滴定是分析化学中重要的分析方法之一,根据其原理回答下列问题:
Ⅰ.酸碱中和滴定是最基本的滴定方法:
(1)滴定管是酸碱中和滴定中重要的仪器,向25mL碱式滴定管中加入氢氧化钠溶液,开始时滴定管的读数为0.00mL,将滴定管中的液体全部放出,放出氢氧化钠溶液的体积为____ (填“大于”“小于”或“等于”)25.00mL。
(2)向碱式滴定管中注入未知浓度氢氧化钠溶液之前的一步操作为____ 。
(3)用已知浓度盐酸滴定未知浓度氢氧化钠溶液的过程中,眼睛应注视____ 。
(4)由表可知,3次滴定中,有一次滴定所用盐酸体积明显偏差,其可能的原因是____ 。
a.锥形瓶用待测液润洗
b.滴定过程中锥形瓶中溶液溅出瓶外
c.滴定前滴定管尖嘴有气泡,滴定结束气泡消失
d.滴定结束时,俯视读数
Ⅱ.高锰酸钾常用于亚硝酸盐的测定。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.02000mol·L-1KMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。反应方程式:2KMnO4+5NaNO2+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O。
(5)在进行滴定操作时,KMnO4溶液盛装在____ (填“酸式”或“碱式”)滴定管中。
(6)达到滴定终点时的现象是____ 。
(7)测得该样品中NaNO2的质量分数为____ 。
Ⅰ.酸碱中和滴定是最基本的滴定方法:
(1)滴定管是酸碱中和滴定中重要的仪器,向25mL碱式滴定管中加入氢氧化钠溶液,开始时滴定管的读数为0.00mL,将滴定管中的液体全部放出,放出氢氧化钠溶液的体积为
(2)向碱式滴定管中注入未知浓度氢氧化钠溶液之前的一步操作为
(3)用已知浓度盐酸滴定未知浓度氢氧化钠溶液的过程中,眼睛应注视
(4)由表可知,3次滴定中,有一次滴定所用盐酸体积明显偏差,其可能的原因是
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 2.10 | 24.20 |
| 第三次 | 10.00 | 4.10 | 24.00 |
b.滴定过程中锥形瓶中溶液溅出瓶外
c.滴定前滴定管尖嘴有气泡,滴定结束气泡消失
d.滴定结束时,俯视读数
Ⅱ.高锰酸钾常用于亚硝酸盐的测定。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.02000mol·L-1KMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液VmL。反应方程式:2KMnO4+5NaNO2+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O。
(5)在进行滴定操作时,KMnO4溶液盛装在
(6)达到滴定终点时的现象是
(7)测得该样品中NaNO2的质量分数为
某同学探究Cu与NO的反应,查阅资料:①Cu与NO反应可生成CuO和N2,②酸性条件下,NO或NO 都能与MnO
都能与MnO 反应生成NO
反应生成NO 和Mn2+
和Mn2+
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式______________ 。
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:

①使用铜丝的优点是______ ; 装置E的作用为_____________________ 。
②装置C中盛放的药品可能是_____________________ ;
③装置D中的现象是____________ ;装置F中反应的离子方程式是_____________________ 。
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。取25.00ml混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
第一次实验数据出现异常,造成这种异常的原因可能是_________ (填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.锥形瓶洗净后用待测液润洗
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:

①使用铜丝的优点是
②装置C中盛放的药品可能是
③装置D中的现象是
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。取25.00ml混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.锥形瓶洗净后用待测液润洗
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


