解答题-原理综合题 适中0.65 引用1 组卷63
油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036kJ•mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH 2=94kJ•mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH 3=-484kJ•mol-1
计算H2S热分解反应④2H2S(g)=S2(g)+2H2(g)的ΔH 4=______ kJ•mol-1。
(2)在1470K、100kPa反应条件下,将n(H2S):n(Ar)=1:4的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为______ ,用各物质的平衡分压表示总反应的平衡常数,表达式Kp=______ ,平衡常数Kp=______ kPa。已知:气体分压(p分)=气体总压(p总)×物质的量分数
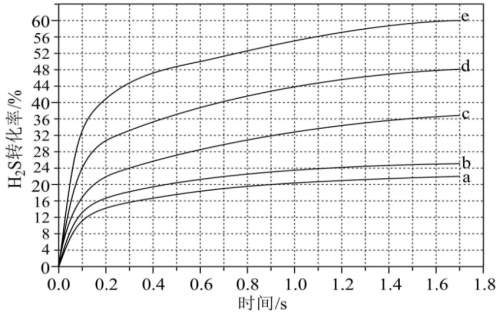
(3)在1373K、100kPa反应条件下,对于n(H2S):n(Ar)分别为4:1、1:1、1:4、1:9、1:19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示:
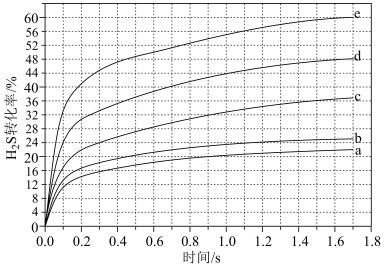
①n(H2S):n(Ar)为4:1和1:1相比,H2S平衡转化率高的是______ ,理由是______ 。
②n(H2S):n(Ar)=1:9对应图中曲线_____ 。
(1)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036kJ•mol-1
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH 2=94kJ•mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH 3=-484kJ•mol-1
计算H2S热分解反应④2H2S(g)=S2(g)+2H2(g)的ΔH 4=
(2)在1470K、100kPa反应条件下,将n(H2S):n(Ar)=1:4的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为
(3)在1373K、100kPa反应条件下,对于n(H2S):n(Ar)分别为4:1、1:1、1:4、1:9、1:19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图所示:

①n(H2S):n(Ar)为4:1和1:1相比,H2S平衡转化率高的是
②n(H2S):n(Ar)=1:9对应图中曲线
23-24高二上·陕西西安·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网