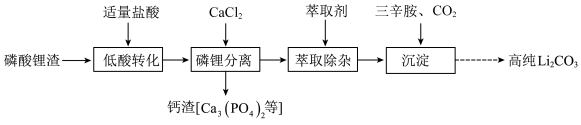
解答题-实验探究题 较难0.4 引用1 组卷186
(1)
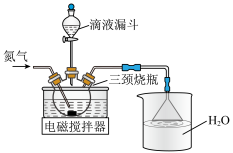
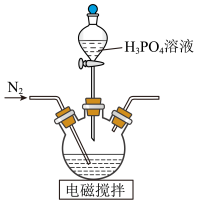
①滴液漏斗中的溶液是
②
③在氮气氛围下,粗产品经150℃干燥、高温焙烧,即可得到锂离子电池的正极材料。焙烧时常向其中加入少量活性炭黑,其主要目的是
(2)
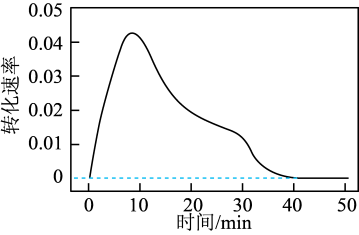
①其他条件不变时,磷酸与水的混合比例对铁粉溶解速率的影响如图所示:
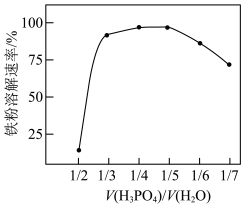
当
②为使反应过程中的
a.用
c.缓慢滴加
③将
23-24高三上·江苏连云港·期中
类题推荐
随着“碳中和”“碳达峰”政策的落实,新能源汽车得到极大发展。磷酸铁(FePO4)可用来制备电动汽车锂离子电池的电极材料,工业上常以硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)为原料经过如下步骤制备磷酸铁(FePO4)。
资料:几种金属离子沉淀的pH:
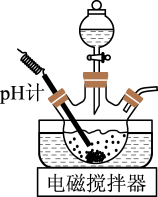
I.如图所示连接装置,将一定量焙烧后的硫铁矿粉末加入三颈烧瓶中,通过:向三颈烧瓶中缓慢加入一定浓度的稀硫酸,50~60℃加热,充分反应,过滤。

II.向滤液中加入FeS固体,充分搅拌至溶液中Fe3+全部被还原。
III.向还原后的溶液中加入FeCO3固体,不断搅拌,使A13+完全转化为Al(OH)3,过滤,得FeSO4溶液。
IV.向除铝后的溶液中加入一种“绿色氧化剂”,充分反应,使FeSO4溶液全部被氧化为Fe2(SO4)3溶液。
V.向含有Fe3+的溶液中加入一定量的Na2HPO4溶液(溶液显碱性),搅拌、过滤、洗涤、干燥得到FePO4·2H2O。
回答下列问题:
(1)步骤I的实验装置中仪器a的名称是____ ,在该步反应过程中温度不宜过高的原因可能是___________ 。
(2)步骤II中还原Fe3+的目的是____ ,检验Fe3+全部被还原的实验操作是___________ 。
(3)步骤III中加入FeCO3的作用是___________ 。(用离子方程式表示)
(4)步骤IV中,加入的“绿色氧化剂”是___________ 。(填化学式)
(5)步骤V中,反应后Fe3+沉淀完全(c≤1×10-5mol·L-1)时,c(PO )最小为
)最小为___________ mol·L-1,已知常温下,Ksp(FePO4)=1.3×10-22。
(6)实验中制得的FePO4与Li2CO3在高温条件下与H2C2O4煅烧可得LiFePO4,其常用作锂离子电池电极材料,如图为Ca-LiFePO4可充电电池的工作原理示意图,锂离子导体膜只允许Li+通过。则放电时,电池的总反应式为___________ 。

资料:几种金属离子沉淀的pH:
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 4.1 | 9.7 | 5.2 |

II.向滤液中加入FeS固体,充分搅拌至溶液中Fe3+全部被还原。
III.向还原后的溶液中加入FeCO3固体,不断搅拌,使A13+完全转化为Al(OH)3,过滤,得FeSO4溶液。
IV.向除铝后的溶液中加入一种“绿色氧化剂”,充分反应,使FeSO4溶液全部被氧化为Fe2(SO4)3溶液。
V.向含有Fe3+的溶液中加入一定量的Na2HPO4溶液(溶液显碱性),搅拌、过滤、洗涤、干燥得到FePO4·2H2O。
回答下列问题:
(1)步骤I的实验装置中仪器a的名称是
(2)步骤II中还原Fe3+的目的是
(3)步骤III中加入FeCO3的作用是
(4)步骤IV中,加入的“绿色氧化剂”是
(5)步骤V中,反应后Fe3+沉淀完全(c≤1×10-5mol·L-1)时,c(PO
(6)实验中制得的FePO4与Li2CO3在高温条件下与H2C2O4煅烧可得LiFePO4,其常用作锂离子电池电极材料,如图为Ca-LiFePO4可充电电池的工作原理示意图,锂离子导体膜只允许Li+通过。则放电时,电池的总反应式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网