填空题 适中0.65 引用1 组卷37
根据要求,回答下列问题:
Ⅰ.已知HClO是比 还弱的酸,氯水中存在下列平衡:
还弱的酸,氯水中存在下列平衡: 、
、 。
。
(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
(2)由此说明在实验室里可用排饱和食盐水法收集 的理由是
的理由是___________ 。
Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
(3)常温下,浓度相同的四种酸溶液① 、②
、② 、③
、③ 、④
、④ ,pH值由大到小的顺序是
,pH值由大到小的顺序是___________ (用序号表示)。
(4)常温下,已知某浓度的 溶液pH=9,该溶液中由水电离出的
溶液pH=9,该溶液中由水电离出的
___________ 。
(5)浓度相同的六种溶液① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其碱性由强到弱的顺序是
,其碱性由强到弱的顺序是___________ (用序号表示);其中 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是___________ 。
(6)浓度均为 的三种溶液①
的三种溶液① 、②
、② 、③
、③ ,这三种溶液中
,这三种溶液中 从大到小的顺序为
从大到小的顺序为___________ (用序号表示)。
Ⅰ.已知HClO是比
(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
| A. | B. | C.HCl | D.NaOH |
Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
(4)常温下,已知某浓度的
(5)浓度相同的六种溶液①
(6)浓度均为
23-24高二上·河南平顶山·阶段练习
类题推荐
已知部分弱酸的电离平衡常数如下表,根据表中数据回答下列问题。
(1)体积相同、pH相同的三种酸溶液①HCOOH ②HCN ③HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是_______ (用序号表示)。
(2)25℃已知某浓度的HCOONa溶液pH=9,原因是_______ 。(用离子方程式表示),该溶液中由水电离出的OH-浓度为_______ 。
(3)浓度相同的四种溶液①HCOONa ②NaCN ③NaHCO3 ④Na2CO3,其碱性由强到弱的顺序是_______ (用序号表示);其中HCOONa溶液中各离子浓度由大到小的顺序是_______ 。
(4)浓度均为0.1mol·L-1三种溶液①HCOONH4、②NH4CN、③NH4HCO3,这三种溶液中c(NH )从大到小的顺序为
)从大到小的顺序为_______ (用序号表示)。
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25°C) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
(1)体积相同、pH相同的三种酸溶液①HCOOH ②HCN ③HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是
(2)25℃已知某浓度的HCOONa溶液pH=9,原因是
(3)浓度相同的四种溶液①HCOONa ②NaCN ③NaHCO3 ④Na2CO3,其碱性由强到弱的顺序是
(4)浓度均为0.1mol·L-1三种溶液①HCOONH4、②NH4CN、③NH4HCO3,这三种溶液中c(NH
已知部分弱酸的电离平衡常数如下表,根据表中数据回答下列问题。
(1)体积相同、pH相同的三种酸溶液①HCOOH ②HCN ③HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是_______ (用序号表示)。
(2)25℃已知某浓度的HCOONa溶液pH=9,该溶液中由水电离出的OH-浓度为_______ 。
(3)25℃时某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO ):c(HCO
):c(HCO )=
)=_______ 。
(4)25℃时,有0.1mol·L-1的四种溶液:①HCl②Na2CO3③HCOOH④NaOH。上述四种溶液中,其中水的电离程度最大的是_______ (填序号,下同),溶液的pH值由大到小的顺序是_______ 。
(5)浓度相同的四种溶液①HCOONa ②NaCN ③NaHCO3 ④Na2CO3,其碱性由强到弱的顺序是_______ (用序号表示)。
(6)浓度均为0.1mol·L-1三种溶液①HCOONH4、②NH4CN、③NH4HCO3,这三种溶液中c(NH )从大到小的顺序为
)从大到小的顺序为_______ (用序号表示)。
(7)向氯化铝溶液中加入偏铝酸钠反应的离子方程式为:_______ 。
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25°C) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
(1)体积相同、pH相同的三种酸溶液①HCOOH ②HCN ③HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的顺序是
(2)25℃已知某浓度的HCOONa溶液pH=9,该溶液中由水电离出的OH-浓度为
(3)25℃时某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO
(4)25℃时,有0.1mol·L-1的四种溶液:①HCl②Na2CO3③HCOOH④NaOH。上述四种溶液中,其中水的电离程度最大的是
(5)浓度相同的四种溶液①HCOONa ②NaCN ③NaHCO3 ④Na2CO3,其碱性由强到弱的顺序是
(6)浓度均为0.1mol·L-1三种溶液①HCOONH4、②NH4CN、③NH4HCO3,这三种溶液中c(NH
(7)向氯化铝溶液中加入偏铝酸钠反应的离子方程式为:
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如表:
① 溶液和
溶液和 溶液中,
溶液中,
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②常温下,pH相同的三种溶液:A. B. NaCN C.
B. NaCN C. ,其物质的量浓度由大到小的顺序是
,其物质的量浓度由大到小的顺序是_______ (填编号)。
③室温下,一定浓度的 溶液pH=9,溶液中
溶液pH=9,溶液中 =
=_______ 。
④将少量 通入NaCN溶液,反应的离子方程式是
通入NaCN溶液,反应的离子方程式是_______ 。
(2)室温下, 通入NaOH溶液中,在所得溶液中
通入NaOH溶液中,在所得溶液中 ,溶液的pH=
,溶液的pH=_______ 。(室温下, 的
的 ;
; )
)
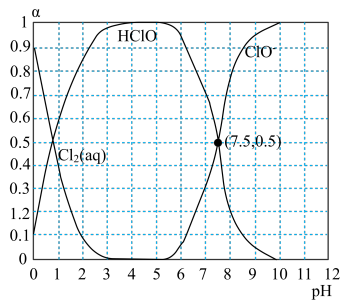
(3)已知25℃氯水溶液中 、HClO和
、HClO和 分别所占分数
分别所占分数 随pH变化的关系如图所示。由图可知该温度下HClO的电离常数值为
随pH变化的关系如图所示。由图可知该温度下HClO的电离常数值为_______ 。
(4)已知:常温下



则 溶液的pH
溶液的pH_______ 7(填“>”“<”或“=”)。
(5)已知25℃时 ,此温度下若在实验室中配制
,此温度下若在实验室中配制 溶液,为使配制过程中不出现浑浊现象,则至少需要加入
溶液,为使配制过程中不出现浑浊现象,则至少需要加入_______  的盐酸(忽略加入盐酸时溶液体积的变化)。
的盐酸(忽略加入盐酸时溶液体积的变化)。
(6) 尾气常用NaOH溶液吸收,生成
尾气常用NaOH溶液吸收,生成 和
和 。已知
。已知 的水解常数
的水解常数 ,常温下某
,常温下某 和
和 混合溶液的pH为5,则混合溶液中
混合溶液的pH为5,则混合溶液中 和
和 的比值为
的比值为_______ 。
(1)已知部分弱酸的电离常数如表:
弱酸 | HCN | ||
电离常数(25℃) |
①
②常温下,pH相同的三种溶液:A.
③室温下,一定浓度的
④将少量
(2)室温下,
(3)已知25℃氯水溶液中

(4)已知:常温下
则
(5)已知25℃时
(6)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


