解答题-工业流程题 困难0.15 引用1 组卷400
某废钒渣(主要成分为V2O3,含有少量Al2O3、CaO)为原料生产V2O5的工艺流程如图:
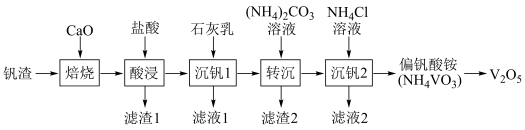
已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为_______ 。
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为_______ 。
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是_______ 。
(4)反应Ca3(VO4)2(s)+3 (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为_______ (用含m,n的代数式表示),已知:Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n。
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是_______ 。
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知 被还原为Mn2+,假设杂质不参与反应。
被还原为Mn2+,假设杂质不参与反应。
①滴定时装KMnO4溶液为_______ 滴定管(填“酸式”或“碱式”)
②则产品中V2O5的质量分数是_______ (V2O5的摩尔质量为Mg·mol-1)。
(7)下列操作会导致测定的纯度偏高的是_______。

已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | V2O | VO |
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是
(4)反应Ca3(VO4)2(s)+3
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO
①滴定时装KMnO4溶液为
②则产品中V2O5的质量分数是
(7)下列操作会导致测定的纯度偏高的是_______。
| A.锥形瓶水洗后未干燥 |
| B.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| C.滴定终点时俯视读数 |
| D.滴定管用蒸馏水洗净后未用标准溶液润洗 |
23-24高二上·湖南邵阳·期中
类题推荐
某废钒渣(主要成分为V2O3,含有少量Al2O3、CaO)为原料生产V2O5的工艺流程如图:
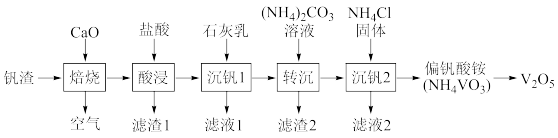
已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
(1)“酸浸”前需将块状固体粉碎,其目的是____ 。
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为____ 。
(3)Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n;则反应Ca3(VO4)2(s)+3CO
 2VO
2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为____ 。(用含m、n的代数式表示)
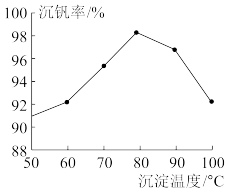
(4)“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是___ 。
(5)NH4VO3灼烧脱氨可得V2O5。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为____ 。
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLc1mol·L-1(NH4)2Fe(SO4)2溶液(VO +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO 被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是
被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是____ (V2O5的摩尔质量为Mg·mol-1)。

已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | VO | V2O | VO |
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为
(3)Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n;则反应Ca3(VO4)2(s)+3CO
(4)“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是

(5)NH4VO3灼烧脱氨可得V2O5。在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLc1mol·L-1(NH4)2Fe(SO4)2溶液(VO
某废钒渣(主要成分为V2O3,含有少量Al2O3、CaO)为原料生产V2O5的工艺流程如图:
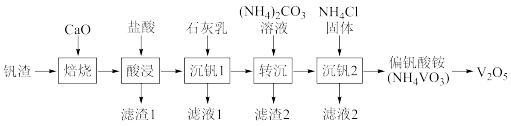
已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表:
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为_______ 。
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为_______ 。
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是_______ 。
(4)反应Ca3(VO4)2(s)+3CO (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为_______ (用含m、n的代数式表示),已知:Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n。
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是_______ 。

已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | VO | V2O | VO |
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是
(4)反应Ca3(VO4)2(s)+3CO
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是
工业上用含三价钒(V2O3)为主的某石煤为原料(含有 Al2O3、CaO 等杂质),钙化法焙烧制备 V2O5,其流程如下:

【资料】+5 价钒在溶液中的主要存在形式与溶液 pH 的关系:
(1)焙烧: 向石煤中加生石灰焙烧,将 V2O3转化为 Ca(VO3)2的化学方程式是______________ 。
(2)酸浸:①Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 pH=4,Ca(VO3)2溶于盐酸的离子方程式是________ 。
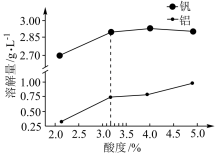
②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约 3.2%,根据下图推测,酸浸时不选择更高酸度的原因是________________ 。
(3)转沉: 将浸出液中的钒转化为 NH4VO3固体,其流程如下:

①浸出液中加入石灰乳的作用是_____ 。
②向(NH4)3VO4溶液中加入 NH4Cl 溶液,控制溶液的 pH=7.5。当 pH>8 时,NH4VO3的产量明显降低,原因是_______________ 。
(4)测定产品中 V2O5的纯度:称取 ag 产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入 b1mLc1mol/L(NH4)2Fe(SO4)2溶液(VO2++2H++Fe2+=VO2++Fe3++H2O) 最后用 c2mol/LKMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗 KMnO4溶液的体积为 b2mL。已知 MnO4-被还原为 Mn2+,假设杂质不参与反应。则产品中 V2O5的质量分数是_____ 。(V2O5的摩尔质量::182g/mol)

【资料】+5 价钒在溶液中的主要存在形式与溶液 pH 的关系:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO2+ | VO3- | V2O74- | VO43- |
(2)酸浸:①Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 pH=4,Ca(VO3)2溶于盐酸的离子方程式是
②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约 3.2%,根据下图推测,酸浸时不选择更高酸度的原因是

(3)转沉: 将浸出液中的钒转化为 NH4VO3固体,其流程如下:

①浸出液中加入石灰乳的作用是
②向(NH4)3VO4溶液中加入 NH4Cl 溶液,控制溶液的 pH=7.5。当 pH>8 时,NH4VO3的产量明显降低,原因是
(4)测定产品中 V2O5的纯度:称取 ag 产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入 b1mLc1mol/L(NH4)2Fe(SO4)2溶液(VO2++2H++Fe2+=VO2++Fe3++H2O) 最后用 c2mol/LKMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗 KMnO4溶液的体积为 b2mL。已知 MnO4-被还原为 Mn2+,假设杂质不参与反应。则产品中 V2O5的质量分数是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


