填空题 较易0.85 引用2 组卷69
Ⅰ.在密闭容器中充入1mol H2和1mol I2,一定温度下发生反应:H2(g)+I2(g)  2HI(g)
2HI(g)
(1)保持容器内气体压强不变,向其中充入1 mol N2,反应速率___________ 。(填“变大”“变小”或“不变”,下同);
(2)保持容器体积不变,向其中充入1 mol N2,反应速率___________ 。
Ⅱ.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(3)该反应化学平衡常数的表达式:K=___________ ;
(4)该反应为___________ (填“吸热”或“放热”)反应;
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为___________ ℃。
(1)保持容器内气体压强不变,向其中充入1 mol N2,反应速率
(2)保持容器体积不变,向其中充入1 mol N2,反应速率
Ⅱ.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)该反应化学平衡常数的表达式:K=
(4)该反应为
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为
23-24高二上·黑龙江齐齐哈尔·阶段练习
类题推荐
在一定体积的密闭容器中,进行如下化学反应:CO2 (g) +H2(g)⇌CO (g) +H2O (g)。其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K =_________ 。
(2)该反应为_______ 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是______ (多选扣分)
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2) =c(CO)
e.容器中的气体密度保持不变
(4)起始时按1:1的比例向容器中充入CO2和H2,保持反应温度为700℃,当反应达到平衡时,c (CO2):c (H2):c (CO):c(H2O) =_______ 。
(5)某温度下,平衡浓度符合下式:c (CO2)·c (H2) =c (CO)·c(H2O),试判断此时的温度为____ ℃。该温度时,若投入的CO2,H2,CO,H2O的浓度分别是2mol/L、3mol/L、6mol/L、1mol/L,则此时平衡向哪个方向哪个方向移动_______ (填正移、逆移、不移动)
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.64 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2) =c(CO)
e.容器中的气体密度保持不变
(4)起始时按1:1的比例向容器中充入CO2和H2,保持反应温度为700℃,当反应达到平衡时,c (CO2):c (H2):c (CO):c(H2O) =
(5)某温度下,平衡浓度符合下式:c (CO2)·c (H2) =c (CO)·c(H2O),试判断此时的温度为
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
请回答下列问题:
(1)该反应为___________反应。(填“吸热”或“放热”)
(2)830℃,c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, C(H2)=0.05mol/L,该反应__________(填“是”或“否”)达到的化学平衡状态。
(3)800℃时,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)=0.01 mol/L,c(H2O)=0.03 mol/L,c(CO2)=0.01 mol/L,c(H2)=0.05 mol/L,则反应开始时,H2O的消耗速率比生成速率___________(填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为___________,H2的转化率为___________(用分数表示)。若再充入1mol H2则H2的转化率为___________(增大,减少,不变)
 CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应为___________反应。(填“吸热”或“放热”)
(2)830℃,c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, C(H2)=0.05mol/L,该反应__________(填“是”或“否”)达到的化学平衡状态。
(3)800℃时,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)=0.01 mol/L,c(H2O)=0.03 mol/L,c(CO2)=0.01 mol/L,c(H2)=0.05 mol/L,则反应开始时,H2O的消耗速率比生成速率___________(填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为___________,H2的转化率为___________(用分数表示)。若再充入1mol H2则H2的转化率为___________(增大,减少,不变)
Ⅰ、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌ CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应为____________ 反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_________ 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_________ ℃。
Ⅱ、向一体积不变的密闭容器中充入2 mol A、0.6 mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g) ⇌3C(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出。图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种不同 的条件。
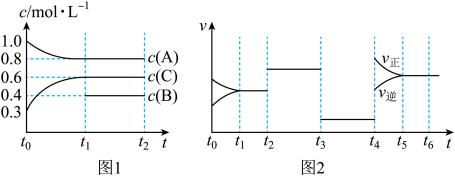
(1)若t1=15 min,则t0~t1阶段以C的浓度变化表示的反应速率V(C)=_____ 。
(2)t3时改变的条件为___________ ,B的起始物质的量为_______ 。
(3)t4~t5阶段,若A的物质的量减少了0.01 mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式___________________ 。
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
Ⅱ、向一体积不变的密闭容器中充入2 mol A、0.6 mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g) ⇌3C(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出。图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种

(1)若t1=15 min,则t0~t1阶段以C的浓度变化表示的反应速率V(C)=
(2)t3时改变的条件为
(3)t4~t5阶段,若A的物质的量减少了0.01 mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


