解答题-工业流程题 适中0.65 引用1 组卷47
研究发现,Cu/Al(OH)3催化剂在工业上有着巨大作用。现以硫酸烧渣(主要成分为Fe2O3、Al2O3、CuO和SiO2等)为原料制备Cu/ Al(OH)3催化剂,流程如图所示:
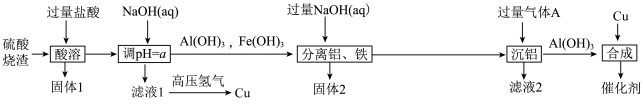
已知常温下,①几种金属离子沉淀的pH如表所示:
②电离常数 H2CO3 Ka1=4.4×10-7 Ka2=4.7×10-11
③A为无色无味气体
回答下列问题:
(1)举一个“固体1”的用途___________ ,“固体2”灼烧产物是___________ (填名称),“分离铝、铁”的操作名称为___________ 。
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度不能太高,其原因是___________ 。
(3)a的范围为___________ , “滤液1”中通入高压氢制备铜的离子方程式为___________ 。
(4)“沉铝”的离子方程式为___________ ,“滤液2”的pH___________ 7(25℃) (填“>”“<”或“=”),判断依据是___________ 。
(5)合成催化剂 ,测定Cu与Al(OH)3的比例:将制得的“催化剂Cu/Al(OH)3”在空气中充分灼烧为CuO和Al2O3,固体质量不改变,则催化剂中n(Cu) : n[Al(OH)3]=___________ 。

已知常温下,①几种金属离子沉淀的pH如表所示:
| 金属离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀pH | 1.9 | 3.4 | 7.4 |
| 完全沉淀pH | 3.7 | 4.7 | 9.6 |
③A为无色无味气体
回答下列问题:
(1)举一个“固体1”的用途
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度不能太高,其原因是
(3)a的范围为
(4)“沉铝”的离子方程式为
(5)合成催化剂 ,测定Cu与Al(OH)3的比例:将制得的“催化剂Cu/Al(OH)3”在空气中充分灼烧为CuO和Al2O3,固体质量不改变,则催化剂中n(Cu) : n[Al(OH)3]=
23-24高三上·四川遂宁·阶段练习
类题推荐
研究发现,在Cu/Al(OH)3催化剂上使用等离子体催化能将CH4和CO2直接转化为CH3OH和CH3CH2OH,某小组以硫酸烧渣(主要成分为Fe2O3、Al2O3、CuO和SiO2等)制备Cu/ Al(OH)3催化剂的流程如图所示:
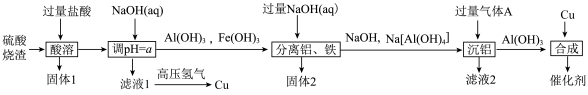
几种金属离子沉淀的pH如表所示:
回答下列问题:
(1)灼烧固体2得到的主要成分是___________ (填化学式)。气体A是___________ (填名称)。
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度,其原因是___________ 。a的范围为___________ 。
(3)滤液1中通入高压氢制备铜的离子方程式为___________ 。
(4)滤液2的pH___________ (填“>”“<”或“=”)7,判断依据是___________ 。
(5)该催化剂能将CH4和CO2转化成CH3OH、CH3CH2OH,这四种分子中属于非极性分子的有___________ (填化学式),能与水分子形成氢键的有___________ (填化学式)。

几种金属离子沉淀的pH如表所示:
| 金属离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀pH | 1.9 | 3.4 | 7.4 |
| 完全沉淀pH | 3.7 | 4.7 | 9.6 |
(1)灼烧固体2得到的主要成分是
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度,其原因是
(3)滤液1中通入高压氢制备铜的离子方程式为
(4)滤液2的pH
(5)该催化剂能将CH4和CO2转化成CH3OH、CH3CH2OH,这四种分子中属于非极性分子的有
研究发现,在 催化剂上使用等离子体催化能将
催化剂上使用等离子体催化能将 和
和 直接转化为
直接转化为 和
和 。某小组以硫酸烧渣(主要成分为
。某小组以硫酸烧渣(主要成分为 和
和 等)制备
等)制备 催化剂的流程如图所示:
催化剂的流程如图所示:
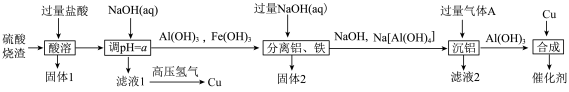
几种金属离子沉淀的pH如表所示:
回答下列问题:
(1)灼烧固体2得到的主要成分是___________ (填化学式)。气体A是_________ (填名称)。
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度,其原因是____________________ 。a的范围为____________________ 。
(3)滤液1中通入高压氢制备铜的离子方程式为_______________________ 。
(4)滤液2的pH__________________ (填“>”“<”或“=”)7。
(5)该催化剂能将 和
和 转化成
转化成 、
、 ,这四种分子中能与水分子形成氢键的有
,这四种分子中能与水分子形成氢键的有______________________ (填化学式)。

几种金属离子沉淀的pH如表所示:
| 金属离子 | |||
| 开始沉淀pH | 1.9 | 3.4 | 7.4 |
| 完全沉淀pH | 3.7 | 4.7 | 9.6 |
(1)灼烧固体2得到的主要成分是
(2)“酸溶”中,适当加热可提高反应速率,但是要控制温度,其原因是
(3)滤液1中通入高压氢制备铜的离子方程式为
(4)滤液2的pH
(5)该催化剂能将
磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
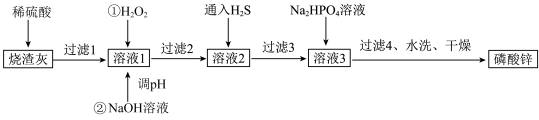
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如下表所示:
(1)写出通入H2S所发生的离子反应方程式___________
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是___________ (填一条)。
(3)加入H2O2的作用___________ 。
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(5)加入Na2HPO4溶液发生反应的离子方程式为___________ 。
(6)洗涤磷酸锌沉淀时应选用___________ (填“冷水”或“热水”)。
(7)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)= 6.3×10-15mol·L-1,则CuS的溶度积Ksp=___________ (已知: 25℃时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶1”中几种金属离子开始沉淀与沉淀完全的pH如下表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 沉淀完全的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)用硫酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是
(3)加入H2O2的作用
(4)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(5)加入Na2HPO4溶液发生反应的离子方程式为
(6)洗涤磷酸锌沉淀时应选用
(7)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1mol·L-1,此时溶液中c(Cu2+)= 6.3×10-15mol·L-1,则CuS的溶度积Ksp=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


