填空题 适中0.65 引用1 组卷55
如图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-(配离子)物质的量浓度的对数。
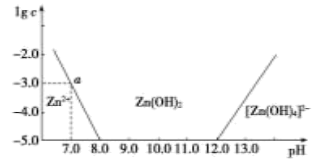
回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为___________ 。
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=___________ 。
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是___________ 。
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH___________ mol(精确到小数点后2位)。

回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH
24-25高二上·全国·假期作业
类题推荐
已知锌及其化合物的性质与铝及其化合物相似。下图横坐标为溶液的pH值,纵坐标为Zn2+或Zn(OH)42-的物质的量浓度的对数。下列说法中不正确的是
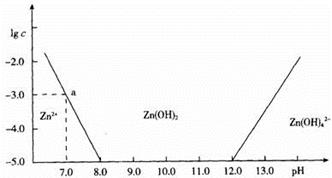

| A.在该温度下,Zn(OH)2的溶度积(Ksp)为1×10―17 |
| B.往1.0L 1.0mol/LZnCl2溶液中加入NaOH固体至pH=6,需NaOH 2.0 mol |
| C.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式为:Zn2++ 4OH―=[Zn(OH)4]2- |
| D.某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围为8.0~12.0 |
已知锌及其化合物的性质与铝及其化合物相似。如图,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-的物质的量浓度(假设Zn2+浓度为10-5 mol·L-1时,Zn2+已沉淀完全)。下列说法不正确的是( )
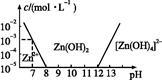

| A.往ZnCl2溶液中加入足量氢氧化钠溶液,离子方程式为Zn2++4OH-=[Zn(OH)4]2- |
| B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 |
| C.某废液中含Zn2+,沉淀Zn2+可以控制溶液pH的范围是8~12 |
| D.向1 L 1 mol·L-1 ZnCl2溶液中加入NaOH固体至pH=6,需NaOH 2 mol |
如下图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-的物质的量浓度的对数.
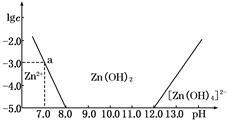
回答下列问题:
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为_______________ 。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=____________________ 。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液中pH的范围是__________________ 。
(4)25℃时,PbCl2浓度随盐酸浓度变化如下表:
根据上表数据判断下列说法正确的是________ 。

回答下列问题:
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液中pH的范围是
(4)25℃时,PbCl2浓度随盐酸浓度变化如下表:
| c(HCl) | |||||||
| (mol/L) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| 103c(PbCl2) | |||||||
| (mol/L) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
根据上表数据判断下列说法正确的是
| A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大 |
| B.PbCl2固体在0.50 mol/L盐酸中的溶解度小于在纯水中的溶解度 |
| C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(络合离子) |
| D.PbCl2固体可溶于饱和食盐水 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


