解答题-结构与性质 较难0.4 引用4 组卷351
铜及其化合物具有广泛的应用。请回答:
(1)Cu元素位于周期表___________ 区。
(2)下列说法不正确 的是___________。
(3)高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是___________ 。(已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)
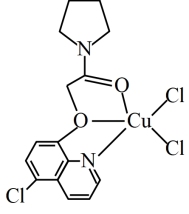
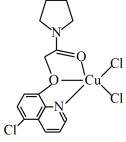
(4) 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是___________ (填标号);1mol配合物中含配位键个数为___________ 。___________ 个。
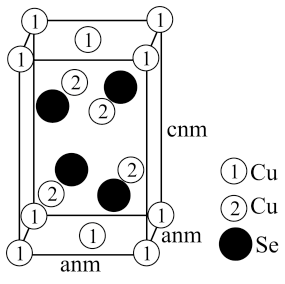
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为___________  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
(1)Cu元素位于周期表
(2)下列说法
| A.基态铜原子的核外电子有29种不同的空间运动状态 |
| B.铜催化烯烃硝化反应时会产生 |
| C. |
| D.配位键的强度: |
(3)高温下固体中
(4)
 )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的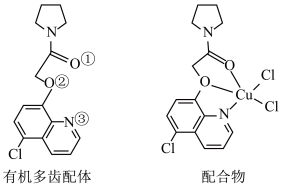
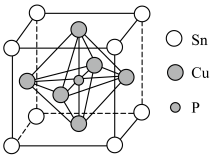
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为
23-24高三上·浙江·期中
类题推荐
回答下列问题:
(1)已知五种气体的溶解度如下表(气体的压强为 ,温度为
,温度为 )。
)。
①比较电负性大小:S_______ P(填“>”“<”或“=”),硫化氢溶解度大于磷化氢可能原因是_______ 。
②已知不同杂化方式的碳原子的电负性会有差异,请从以上信息排出电负性的正确顺序:
_______ 
_______  ,乙烷、乙烯、乙炔中最易与金属钠反应的物质是
,乙烷、乙烯、乙炔中最易与金属钠反应的物质是_______ 。
(2)镍原子形成的微粒,电子排布式分别为① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ ,有关这些微粒的叙述,下列叙述正确的是_______。
,有关这些微粒的叙述,下列叙述正确的是_______。
(3)铜及其化合物具有广泛的应用。请回答:
① 元素位于周期表
元素位于周期表_______ 区。
②下列说法不正确的是_______ 。
A.基态铜原子的核外电子有29种不间的空间运动状态
B.铜催化烯烃硝化反应时会产生 的键角比
的键角比 大
大
C. 中非金属元素电负性:
中非金属元素电负性:
D.配位键的强度: 大于
大于
③高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是_______ 。[已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 的水合能为
的水合能为 的第二电离能为
的第二电离能为 。]
。]
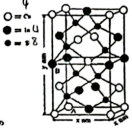
④ 与S形成的某化合物晶体的晶胞如图,该化合物的化学式为
与S形成的某化合物晶体的晶胞如图,该化合物的化学式为_______ 。该晶胞形状为长方体,长为 ,宽为
,宽为 ,高为
,高为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。该晶体的密度为
。该晶体的密度为_______  。
。
(1)已知五种气体的溶解度如下表(气体的压强为
| 气体 | 乙烷 | 乙烯 | 乙炔 | 硫化氢 | 磷化氢 |
| 溶解度 | 0.0062 | 0.0149 | 0.117 | 0.36 | 0.036 |
②已知不同杂化方式的碳原子的电负性会有差异,请从以上信息排出电负性的正确顺序:
(2)镍原子形成的微粒,电子排布式分别为①
| A.微粒半径: | B.由光谱仪一定可以捕捉到发射光谱的是:②③④ |
| C.电离一个电子所需最低能量: | D.得电子能力: |
①
②下列说法不正确的是
A.基态铜原子的核外电子有29种不间的空间运动状态
B.铜催化烯烃硝化反应时会产生
C.
D.配位键的强度:
③高温下固体中
④

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网