解答题-原理综合题 适中0.65 引用1 组卷51
合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是_____ 。
(2)合成氨的反应原理为 ;在一容积为2L的密闭容器中加入一定量的
;在一容积为2L的密闭容器中加入一定量的 和0.5mol
和0.5mol ,在一定条件下发生合成氨反应,反应中
,在一定条件下发生合成氨反应,反应中 的物质的量浓度的变化情况如下图
的物质的量浓度的变化情况如下图
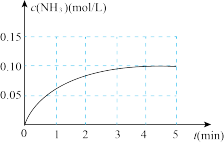
①根据上图,计算从反应开始到平衡时,平均反应速率
_____ 。
②平衡时测得 的物质的量为0.10mol,则的转化率
的物质的量为0.10mol,则的转化率
_____ ,该温度下的平衡常数
_____ 。
(3)对于反应 ,在一定条件下氨的平衡含量如下表。
,在一定条件下氨的平衡含量如下表。
①该反应为_____ (填“吸热”或“放热”)反应。
②其他条件不变时,温度升高,氨的平衡含量减小的原因是_____ 。
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_____ 。
(1)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
| 序号 | 化学反应 | K(298K)的数值 |
| ① | ||
| ② |
(2)合成氨的反应原理为

①根据上图,计算从反应开始到平衡时,平均反应速率
②平衡时测得
(3)对于反应
| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
②其他条件不变时,温度升高,氨的平衡含量减小的原因是
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
23-24高二上·广东广州·期中
类题推荐
合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为_______ 。
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是_______ 。
(3)对于反应N2(g)+3H2(g)⇌2NH3(g),在一定条件下氨的平衡含量如下表。
①该反应为_______ (填“吸热”或“放热”)反应。
②其他条件不变时,温度升高氨的平衡含量减小的原因是_______ (填字母序号)。
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_______ 。
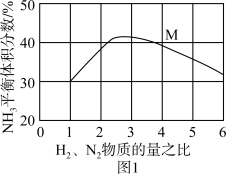
(4)图1表示500℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中M点数据计算N2的平衡体积分数_______ ;
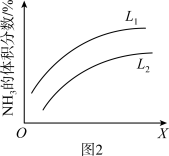
(5)图2是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是___ (填“温度”或“压强”);判断L1、L2的大小关系并说明理由____ 。
(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
序号 | 化学反应 | K(298K)的数值 |
① | N2(g) + O2(g)⇌ 2NO(g) | 5×10-31 |
② | N2(g) + 3H2(g)⇌2NH3(g) | 4.1×106 |
温度/℃ | 压强/MPa | 氨的平衡含量 |
200 | 10 | 81.5% |
550 | 10 | 8.25% |
②其他条件不变时,温度升高氨的平衡含量减小的原因是
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(4)图1表示500℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中M点数据计算N2的平衡体积分数

(5)图2是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是

合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为_______ 。
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是_______ 。
(3)对于反应N2(g)+3H2(g)⇌2NH3(g),在一定条件下氨的平衡含量如下表。
①该反应为_______ (填“吸热”或“放热”)反应。
②其他条件不变时,温度升高氨的平衡含量减小的原因是_______ (填字母序号)。
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是_______ 。
(4)一定温度下,在容积恒定的密闭容器中充入1mol氮气和3mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1mol氮气和3mol氢气,氮气的平衡转化率_______ (填“变大”“变小”或“不变”)。
(5)T℃时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[n(H2)/n(N2)]时某反应物X的平衡转化率变化曲线。

①反应物X是_______ (填“N2”或“H2”)。
②判断依据是_______ 。
(6)在其他条件相同时,下图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示_______ ,其中X1_______ X2(填“>”或“<”)。

(1)反应N2(g)+3H2(g)⇌2NH3(g)的化学平衡常数表达式为
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
| 序号 | 化学反应 | K(298K)的数值 |
| ① | N2(g)+O2(g)⇌2NO(g) | 5×10-31 |
| ② | N2(g)+3H2(g)⇌2NH3(g) | 4.1×106 |
(3)对于反应N2(g)+3H2(g)⇌2NH3(g),在一定条件下氨的平衡含量如下表。
| 温度/℃ | 压强/MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
①该反应为
②其他条件不变时,温度升高氨的平衡含量减小的原因是
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,Q>K,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是
(4)一定温度下,在容积恒定的密闭容器中充入1mol氮气和3mol氢气,一段时间后达化学平衡状态。若保持其他条件不变,向上述平衡体系中再充入1mol氮气和3mol氢气,氮气的平衡转化率
(5)T℃时,在有催化剂的恒容密闭容器中充入N2和H2。下图为不同投料比[n(H2)/n(N2)]时某反应物X的平衡转化率变化曲线。

①反应物X是
②判断依据是
(6)在其他条件相同时,下图为分别测定不同压强、不同温度下,N2的平衡转化率。L表示

合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)反应 的化学平衡常数表达式为
的化学平衡常数表达式为___________ 。
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氨,而没有选用氮气和氧气反应固氮的原因是___________ 。
(3)对于反应 ,在一定条件下氨的平衡含量如下表。
,在一定条件下氨的平衡含量如下表。
①该反应为___________ (填“吸热”或“放热”)反应。
②其他条件不变时,温度升高氨的平衡含量减小的原因是___________ (填字母)。
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大, ,平衡逆向移动
,平衡逆向移动
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是 ,而非
,而非 ,可能的原因是
,可能的原因是___________ 。
(4)下图表示 条件下,原料气投料比与平衡时
条件下,原料气投料比与平衡时 体积分数的关系。根据图中M点数据计算出
体积分数的关系。根据图中M点数据计算出 的平衡体积分数为
的平衡体积分数为___________ 。

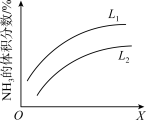
(5)下图是合成氨反应平衡时,混合气中 的体积分数随温度或压强变化的曲线,图中
的体积分数随温度或压强变化的曲线,图中 、X分别代表温度或压强。其中X代表的是
、X分别代表温度或压强。其中X代表的是___________ (填“温度”或“压强”)。
(1)反应
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氨,而没有选用氮气和氧气反应固氮的原因是
| 序号 | 化学反应 | |
| ① | ||
| ② |
(3)对于反应
| 温度/℃ | 压强/ | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
②其他条件不变时,温度升高氨的平衡含量减小的原因是
a.温度升高,正反应速率减小,逆反应速率增大,平衡逆向移动
b.温度升高,浓度商(Q)变大,
c.温度升高,活化分子数增多,反应速率加快
d.温度升高,K变小,平衡逆向移动
③哈伯选用的条件是
(4)下图表示

(5)下图是合成氨反应平衡时,混合气中

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


