填空题 适中0.65 引用1 组卷194
按要求回答下列问题:
(1)pH=13的氢氧化钠与pH=2的硫酸溶液混合,所得混合液的pH= 11,则强碱与强酸的体积比为___________ 。
(2)25℃时,HA的电离常数K=1×10-6,则浓度均为0.01 mol/L的HA与NaA溶液等体积混合,则混合溶液呈___________ (填“酸”“碱”或“中”)性。
(3)79℃,0.01 mol/L的NaOH溶液的pH = 10,此时水的离子积为___________ 0.01mol/L的HB溶液的pH为5,则T℃时HB的电离常数K为___________ 。
(4)亚磷酸(H3PO3)是一种二元弱酸,写出H3PO3与过量NaOH溶液反应的化学方程式___________ 。
(5)25℃时,在浓度均为1 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得其中c( )分别为a、b、c (mol/L),则a、b、c的大小关系
)分别为a、b、c (mol/L),则a、b、c的大小关系___________ 。
(1)pH=13的氢氧化钠与pH=2的硫酸溶液混合,所得混合液的pH= 11,则强碱与强酸的体积比为
(2)25℃时,HA的电离常数K=1×10-6,则浓度均为0.01 mol/L的HA与NaA溶液等体积混合,则混合溶液呈
(3)79℃,0.01 mol/L的NaOH溶液的pH = 10,此时水的离子积为
(4)亚磷酸(H3PO3)是一种二元弱酸,写出H3PO3与过量NaOH溶液反应的化学方程式
(5)25℃时,在浓度均为1 mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得其中c(
23-24高三上·北京·阶段练习
类题推荐
请按要求回答下列问题:
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=__ mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为__ ,由水电离出的c(OH-)=___ mol·L-1。
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数___ (填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是___ 。

(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
①25℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___ 。(用a、b、c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___ 。
③25℃时,等浓度的HCN和NaCN混合溶液显___ 性。(酸、碱、中)
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
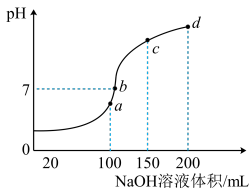
试分析图中a、b、c、d四个点,水的电离程度最大的是__ ;在b点,溶液中各离子浓度由大到小的排列顺序是__ 。
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数

(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
③25℃时,等浓度的HCN和NaCN混合溶液显
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是
25℃时,下表是几种弱酸的电离平衡常数,回答下列问题。
(1)某温度时,水的 ,
, 的NaOH溶液aL与
的NaOH溶液aL与 的
的 溶液bL混合,若所得混合溶液
溶液bL混合,若所得混合溶液 ,则a∶b为
,则a∶b为_______ 。
(2)25℃时,某NaHB与 混合溶液的
混合溶液的 ,求
,求
_______ 。
(3)25℃时,等浓度的三种溶液(A. 溶液、B.NaHD溶液、C.NaA溶液)的pH由大到小的顺序为
溶液、B.NaHD溶液、C.NaA溶液)的pH由大到小的顺序为_______ (填写序号)。
(4)浓度均为 的
的 与
与 的混合溶液中,
的混合溶液中, 、
、 、
、 、
、 浓度从大到小的顺序为
浓度从大到小的顺序为_______ 。
(5)25℃时,等浓度等体积NaHB与 混合溶液显
混合溶液显_______ 性(填“酸”、“碱”或“中”)。
(6)现有浓度为0.02mol/L的HA溶液与0.01mol/LNaOH溶液等体积混合后,下列关系正确的是_______(填标号)。
| 化学式 | HA | |||
| 电离常数 |
(2)25℃时,某NaHB与
(3)25℃时,等浓度的三种溶液(A.
(4)浓度均为
(5)25℃时,等浓度等体积NaHB与
(6)现有浓度为0.02mol/L的HA溶液与0.01mol/LNaOH溶液等体积混合后,下列关系正确的是_______(填标号)。
| A. | B. |
| C. | D. |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


