解答题-原理综合题 较难0.4 引用1 组卷81
“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。烟道气和汽车尾气( 、
、 等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考并回答下列问题:
等)是造成雾霾天气的原因之一,对这些排放气的处理以及再利用是化学工作者研究的重要课题。请思考并回答下列问题:
(1) 在一定条件下可发生分解:
在一定条件下可发生分解: ,一定温度下,在恒容密闭容器中充入一定量
,一定温度下,在恒容密闭容器中充入一定量 进行该反应,能判断反应已达到化学平衡状态的是___________(填字母)。
进行该反应,能判断反应已达到化学平衡状态的是___________(填字母)。
(2) 是用反应体系中气体物质的分压来表示的平衡常数,即将
是用反应体系中气体物质的分压来表示的平衡常数,即将 表达式中平衡浓度用平衡分压代替。已知反应:
表达式中平衡浓度用平衡分压代替。已知反应: ,该反应中正反应速率
,该反应中正反应速率 ,逆反应速率
,逆反应速率 ,其中
,其中 、
、 为速率常数,则
为速率常数,则 为
为___________ (用 、
、 表示)。
表示)。
(3) 时,
时, 与
与 以物质的量
以物质的量 混合,置于某密闭容器中还能发生如下化学反应:
混合,置于某密闭容器中还能发生如下化学反应: ,实验测得该反应速率方程(以
,实验测得该反应速率方程(以 为基准)为
为基准)为 ,
, 。某时刻测得体系中
。某时刻测得体系中 的分压为
的分压为 ,则此时的反应速率为
,则此时的反应速率为___________  。
。
(4)在有氧和新型催化剂作用下, 和
和 可以反应生成
可以反应生成 ,将一定比例的
,将一定比例的 、
、 和
和 通入装有新型催化剂的反应器。测得相同时间内
通入装有新型催化剂的反应器。测得相同时间内 去除率随温度的变化如图所示:
去除率随温度的变化如图所示:
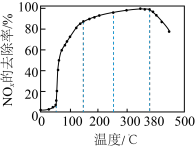
在50~250℃范围内, 的去除率先快速上升后变缓,请你说出变缓的主要原因:
的去除率先快速上升后变缓,请你说出变缓的主要原因:___________ 。
(5)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物 的化学方程式如下:
的化学方程式如下:
Ⅰ.
Ⅱ.
已知:
在1L恒容密闭容器中充入 、
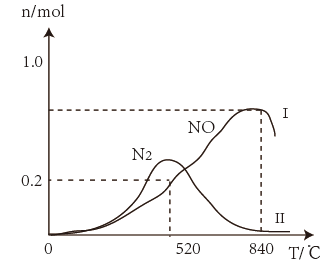
、 ,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示。
,在催化剂作用下发生两个竞争反应Ⅰ、Ⅱ,测得不同温度下反应相同时间有关物质的量关系如图所示。
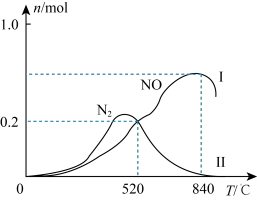
①520℃时, 的有效转化率=
的有效转化率=___________ (保留3位有效数字)。
②工业用氨催化氧化制备 ,选择的最佳温度是
,选择的最佳温度是___________ 。
③520℃时,反应Ⅱ的平衡常数
___________ (保留3位有效数字)。
(1)
| A.容器中压强不再变化 | B.气体的平均相对分子质量保持不变 |
| C. | D.气体的密度保持不变 |
(2)
(3)
(4)在有氧和新型催化剂作用下,

在50~250℃范围内,
(5)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物
Ⅰ.
Ⅱ.
已知:
在1L恒容密闭容器中充入

①520℃时,
②工业用氨催化氧化制备
③520℃时,反应Ⅱ的平衡常数
23-24高二上·福建宁德·期中
类题推荐
烟道气和汽车尾气(NOx、NH3等)是造成雾霾天气的原因之一。对这些排放气的处理以及再利用是化学工作者研究的重要课题。
(1)H2-SCR脱硝
①氢气在富氧条件下催化还原NOx反应在低温时仍具有高活性和选择性,已知催化剂铑(Rh)表面H2催化还原NO的详细反应机理如表所示,其他条件一定时,决定H2催化还原NO反应速率的基元反应为_______ ,基元反应OH(s)+Rh(s)⟹H(s)+O(s)的焓变ΔH=_______ kJ/mol
②1093K时,NO与H2以物质的量2:1混合,置于某密闭容器中还能发生如下化学反应:2NO(g)+H2(g)=N2O(g)+H2O(g),实验测得该反应速率方程(以N2O为基准)为v(N2O)=kp2(NO)p(H2),k=5.6×10-12Pa-2·s-1。某时刻测得体系中NO的分压为2.0kPa,则此时的反应速率为_______ Pa·s-1。
(2)NH3-SCR脱硝
在有氧和新型催化剂作用下,NOx和NH3可以反应生成N2,将一定比例的O2、NOx和NH3通入装有新型催化剂的反应器。测得相同时间内NOx的去除率随温度变化如图所示:_______ ;380℃后去除率下降的可能原因是_______ 。
(3)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物N2的化学方程式如下:
I:
II:
已知:有效转化率=
在1L恒容密闭容器中充入1molNH3、1.45molO2,在催化剂作用下发生两个竞争反应I、II,测得不同温度下反应相同时间有关物质的量关系如图所示:_______ (保留1位小数)。
②工业用氨催化氧化制备HNO3,选择的最佳温度是_______ 。
③520℃时,反应II的平衡常数K=_______ mol·L-1(保留3位有效数字)。
(1)H2-SCR脱硝
①氢气在富氧条件下催化还原NOx反应在低温时仍具有高活性和选择性,已知催化剂铑(Rh)表面H2催化还原NO的详细反应机理如表所示,其他条件一定时,决定H2催化还原NO反应速率的基元反应为
| 基元反应 | 活化能Ea(kJ/mol) |
| NO+Rh(s)⟹NO(s) NO(s)+Rh(s)⟹N(s)+O(s) N(s)+N(s)⟹N2+Rh(s)+Rh(s) H2+Rh(s)+Rh(s)⟹H(s)+H(s) H2O(s)⟹H2O+Rh(s)+Rh(s) H(s)+H(s)⟹H2+Rh(s)+Rh(s) NO(s)⟹NO+Rh(s) OH(s)+Rh(s)⟹H(s)+O(s) H(s)+O(s)⟹OH(s)+Rh(s) OH(s)+H(s)⟹H2O(s)+Rh(s) | 0.0 97.5 120.9 12.6 45.0 77.8 108.9 37.7 83.7 33.5 |
(2)NH3-SCR脱硝
在有氧和新型催化剂作用下,NOx和NH3可以反应生成N2,将一定比例的O2、NOx和NH3通入装有新型催化剂的反应器。测得相同时间内NOx的去除率随温度变化如图所示:

(3)工业上可用“氨催化氧化法”生产NO,以氨气、氧气为原料,在催化剂存在下生成NO和副产物N2的化学方程式如下:
I:
II:
已知:有效转化率=
在1L恒容密闭容器中充入1molNH3、1.45molO2,在催化剂作用下发生两个竞争反应I、II,测得不同温度下反应相同时间有关物质的量关系如图所示:
②工业用氨催化氧化制备HNO3,选择的最佳温度是
③520℃时,反应II的平衡常数K=
造成大气污染的NOx主要来自于汽车尾气的排放,对其如何处理是我们研究的重要课题。
(1)已知:


则用焦炭还原NO生成无污染气体的热化学方程式为_______ 。
(2)在催化剂作用下发生反应: ,在一定温度下,向1L的恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
,在一定温度下,向1L的恒容密闭容器中充入2.0molNO2和2.0molCO,测得相关数据如下:
①其他条件不变,若不使用催化剂,则0~5minNO2的转化率将_______ (填“变大”、“变小”或“不变”)。
②以下表述能说明该反应已达到平衡状态的是_______ 。
A.气体的颜色不再变化 B.CO的反应速率为N2的4倍
C.混合气的压强不再变化 D.化学平衡常数K不再变化
③在20min时,保持温度不变,继续向容器中再加入1.0molNO2和1.0molN2,则化学平衡_______ 移动(填“正向”、“逆向”或“不”)。
(3)有人利用反应 对NO2进行吸附。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强和相同时间下,NO2的转化率与压强的关系如图所示。
对NO2进行吸附。在T℃下,向密闭容器中加入足量的C和一定量的NO2气体,在不同压强和相同时间下,NO2的转化率与压强的关系如图所示。
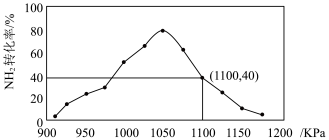
在T℃、1100KPa时,该反应的化学平衡常数
_______  (用平衡分压代替平衡浓度,气体分压=气体总压×体积分数;保留两位小数)。
(用平衡分压代替平衡浓度,气体分压=气体总压×体积分数;保留两位小数)。
(1)已知:
则用焦炭还原NO生成无污染气体的热化学方程式为
(2)在催化剂作用下发生反应:
| 0min | 5min | 10min | 15min | 20min | |
| 2.00 | 1.70 | 1.56 | 1.50 | 1.50 | |
| 0 | 0.15 | 0.22 | 0.25 | 0.25 |
②以下表述能说明该反应已达到平衡状态的是
A.气体的颜色不再变化 B.CO的反应速率为N2的4倍
C.混合气的压强不再变化 D.化学平衡常数K不再变化
③在20min时,保持温度不变,继续向容器中再加入1.0molNO2和1.0molN2,则化学平衡
(3)有人利用反应

在T℃、1100KPa时,该反应的化学平衡常数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网