解答题-工业流程题 较难0.4 引用1 组卷206
锑( )冶炼过程中产生的副产物主要成分为
)冶炼过程中产生的副产物主要成分为 、
、 、
、 和
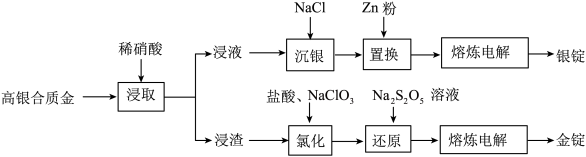
和 等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:
等,因含银量很高,是重要的银提取原料。从该副产物中提取银的工艺流程如下:

已知:①水合肼为 ,有很强的还原性;
,有很强的还原性;
② 在碱性条件下易转化为
在碱性条件下易转化为 ;
;
③常温下, 的溶解度为
的溶解度为 ,
, 的溶解度为0.79g。
的溶解度为0.79g。
回答下列问题:
(1) 的电子式为
的电子式为_______ 。
(2)脱氯渣的主要成分有 、
、 、
、 和
和_______ 。
(3)“还原脱氯”过程中会产生无色无味无毒气体,则 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(4)“氧化分银”中,不直接用硝酸的原因是_______ 。
(5)“氧化分银”中,银被氧化的离子方程式为_______ 。
(6)“沉铅过滤”中主要析出 的原因是
的原因是_______ 。
(7)“沉铅过滤”中硫酸的用量系数对铅和银的沉淀率影响如图所示。
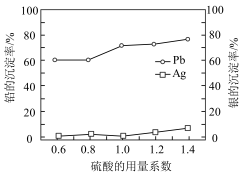
硫酸的用量系数最佳选择是_______ ,理由是_______ 。

已知:①水合肼为
②
③常温下,
回答下列问题:
(1)
(2)脱氯渣的主要成分有
(3)“还原脱氯”过程中会产生无色无味无毒气体,则
(4)“氧化分银”中,不直接用硝酸的原因是
(5)“氧化分银”中,银被氧化的离子方程式为
(6)“沉铅过滤”中主要析出
(7)“沉铅过滤”中硫酸的用量系数对铅和银的沉淀率影响如图所示。

硫酸的用量系数最佳选择是
23-24高三上·湖北·阶段练习
类题推荐
五氧化二钒(V2O5)广泛用于冶金、化工等行业。一种以淅川钒矿(钒以+3、+4价的化合物存在、SiO2、Fe3O4以及Al2O3)为原料生产五氧化二钒的工艺流程如下:
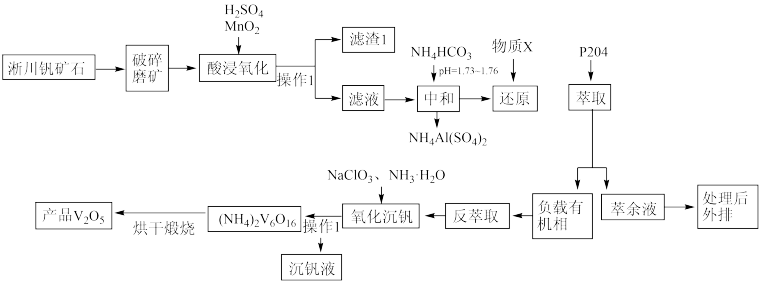
已知:①萃取剂P2O4对VO2+具有高选择性,且萃取Fe3+而不萃取Fe2+、Mn2+、Al3+
②氧化性:VO >Fe3+>VO2+>Fe2+
>Fe3+>VO2+>Fe2+
③萃取反应为:VO2++(HR2PO4)2(O) VO(R2PO4)2(O)+2H+,式中HR2PO4为P2O4,R=C8H17
VO(R2PO4)2(O)+2H+,式中HR2PO4为P2O4,R=C8H17
④
回答下列问题:
(1)“酸浸氧化”中,VO+被氧化成VO2+,同时还有___________ 离子被氧化。写出VO+转化为VO 反应的离子方程式
反应的离子方程式___________ 。
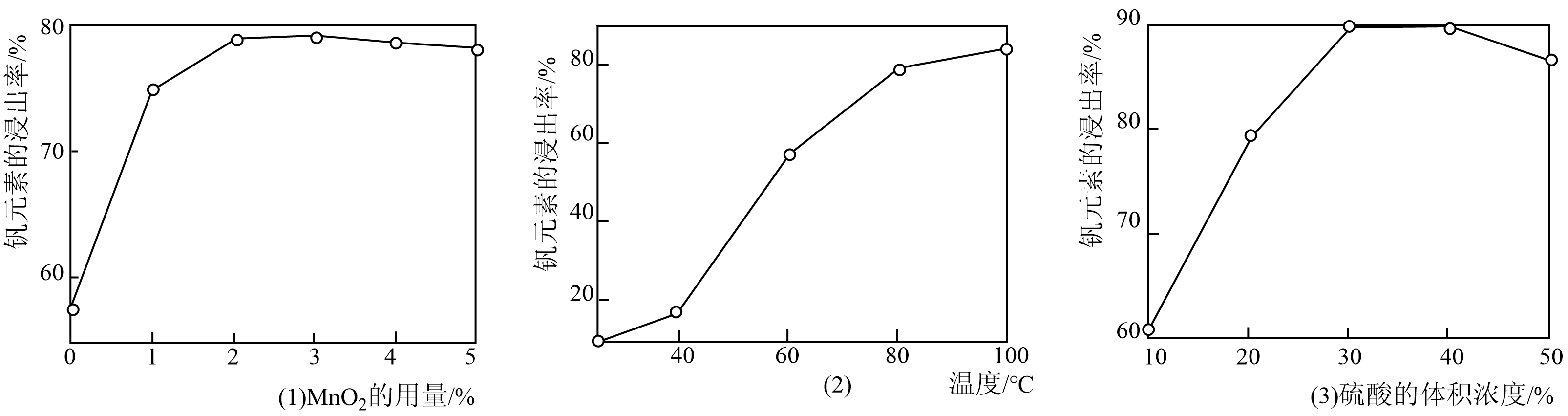
(2)研究表明,“酸浸氧化”中MnO2的用量、温度和硫酸的体积浓度会直接影响钒元素的浸出率,由图(1)(2)(3)可知,最佳条件为___________ (填序号)
(3)“滤渣1”的主要成分为___________ (填化学式)。
(4)“还原”中添加的物质X是___________ (填化学式),且要控制物质X的加入量,既不能过多,也不能过少,原因是___________ 。
(5)“氧化沉钒”的离子方程式是___________ 。
(6)用石灰中和处理萃余液,Fe2+、Al3+、Mn2+以氢氧化物形式沉淀,要使金属离子完全沉淀,则pH的理论最小值为___________ (当溶液中某离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。

已知:①萃取剂P2O4对VO2+具有高选择性,且萃取Fe3+而不萃取Fe2+、Mn2+、Al3+
②氧化性:VO
③萃取反应为:VO2++(HR2PO4)2(O)
④
| 化合物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| 溶度积常数(25℃)近似值 | 10-17 | 10-39 | 10-35 | 10-13 |
(1)“酸浸氧化”中,VO+被氧化成VO2+,同时还有
(2)研究表明,“酸浸氧化”中MnO2的用量、温度和硫酸的体积浓度会直接影响钒元素的浸出率,由图(1)(2)(3)可知,最佳条件为

(3)“滤渣1”的主要成分为
(4)“还原”中添加的物质X是
(5)“氧化沉钒”的离子方程式是
(6)用石灰中和处理萃余液,Fe2+、Al3+、Mn2+以氢氧化物形式沉淀,要使金属离子完全沉淀,则pH的理论最小值为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网