单选题 适中0.65 引用1 组卷130
一定条件下,酸性KMnO4溶液与H2C2O4发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是


| A.Mn(Ⅲ)不能氧化H2C2O4 |
| B.整个滴定过程中,反应速率逐渐减小 |
| C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存 |
| D.总反应为:2MnO |
23-24高二上·福建莆田·期中
类题推荐
定性与定量研究影响化学反应速率的因素实验如下:
实验Ⅰ:测定相同体积的 的硫酸分别与足量锌粒和锌粉反应的速率。
的硫酸分别与足量锌粒和锌粉反应的速率。
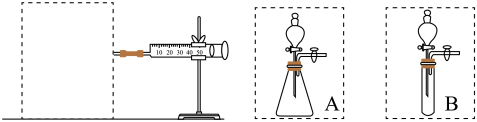
(1)测定实验中为了尽可能排除Zn和H2SO4反应过程中放热带来的影响,虚框内装置应选择上图中的___________ (填“A”或“B”)。
(2)为完成本实验,除图示仪器和用品外,还必需的仪器是___________ 。
(3)根据此实验探究,可以得出的结论是:其他条件不变时,硫酸与锌粉的反应速率___________ 硫酸与锌粒的反应速率(填“大于”、“小于”或“等于”),原因是___________ 。
实验Ⅱ:利用 溶液和酸性
溶液和酸性 溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如下表:
溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如下表:
(4)
___________ ;通过实验①、③可探究___________ 的改变对反应速率的影响。
(5)利用实验②中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
___________ 。
(6)文献记载一定条件下,酸性 溶液与
溶液与 发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。
发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。

下列说法正确的是___________ 。
A.Mn(Ⅲ)不能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
实验Ⅰ:测定相同体积的

(1)测定实验中为了尽可能排除Zn和H2SO4反应过程中放热带来的影响,虚框内装置应选择上图中的
(2)为完成本实验,除图示仪器和用品外,还必需的仪器是
(3)根据此实验探究,可以得出的结论是:其他条件不变时,硫酸与锌粉的反应速率
实验Ⅱ:利用
| 序号 | 温度/K | H2O | 溶液颜色褪至无色时所需时间/s | ||
| V/mL | V/mL | V/mL | |||
| ① | 293 | 2 | 5 | 3 | t1 |
| ② | 293 | V1 | 3 | 5 | 8 |
| ③ | 313 | 2 | 5 | V2 | t2 |
(5)利用实验②中数据计算,用
(6)文献记载一定条件下,酸性

下列说法正确的是
A.Mn(Ⅲ)不能氧化
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
定性与定量研究影响化学反应速率的因素实验如下:
实验Ⅰ:测定相同体积的1mol•L-1硫酸分别与足量锌粒和锌粉反应的速率。

(1)测定实验中为了尽可能排除Zn和H2SO4反应过程中放热带来的影响,虚框内装置应选择图中的________ (填“A”或“B”)。
(2)为完成本实验,除图示仪器和用品外,还必需的仪器是________ 。
(3)根据此实验探究,可以得出的结论是:其他条件不变时,硫酸与锌粉的反应速率_____ 硫酸与锌粒的反应速率(填“大于”、“小于”或“等于”),原因是_______ 。
实验Ⅱ:利用H2C2O4溶液和酸性KMnO4溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如表:
(4)V1=________ ;通过实验①、③可探究________ 的改变对反应速率的影响。
(5)利用实验②中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=________ 。
(6)文献记载一定条件下,酸性KMnO4溶液与H2C2O4发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如图所示。

下列说法正确的是_______ 。
A.Mn(Ⅲ)不能氧化H2C2O4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
实验Ⅰ:测定相同体积的1mol•L-1硫酸分别与足量锌粒和锌粉反应的速率。

(1)测定实验中为了尽可能排除Zn和H2SO4反应过程中放热带来的影响,虚框内装置应选择图中的
(2)为完成本实验,除图示仪器和用品外,还必需的仪器是
(3)根据此实验探究,可以得出的结论是:其他条件不变时,硫酸与锌粉的反应速率
实验Ⅱ:利用H2C2O4溶液和酸性KMnO4溶液之间的反应,探究外界条件改变对化学反应速率的影响。实验如表:
| 序号 | 温度/K | 0.02mol•L-1KMnO4 | 0.1mol•L-1H2C2O4 | H2O | 溶液颜色褪至无色时所需时间/s |
| V/mL | V/mL | V/mL | |||
| ① | 293 | 2 | 5 | 3 | t1 |
| ② | 293 | V1 | 3 | 5 | 8 |
| ③ | 313 | 2 | 5 | V2 | t2 |
(4)V1=
(5)利用实验②中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=
(6)文献记载一定条件下,酸性KMnO4溶液与H2C2O4发生反应,Mn(Ⅱ)起催化作用,过程中不同价态含Mn粒子的浓度随时间变化如图所示。

下列说法正确的是
A.Mn(Ⅲ)不能氧化H2C2O4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


