单选题 较易0.85 引用2 组卷148
用 催化还原法消除氮氧化物,发生反应:
催化还原法消除氮氧化物,发生反应:
 ,相同条件下,在3L恒容密闭容器中,选用不同催化剂,产生
,相同条件下,在3L恒容密闭容器中,选用不同催化剂,产生 的量随时间变化如图所示。下列说法正确的是
的量随时间变化如图所示。下列说法正确的是
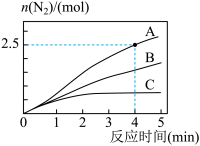

| A.该反应的活化能大小顺序是: |
| B.增加反应物的量,使活化分子百分数增加,有效碰撞增多,反应速率加快 |
| C.当 |
| D.若反应在恒容绝热的密闭容器中进行,当K值不变时,说明已达到平衡 |
23-24高二上·福建福州·期中
类题推荐
在绝热恒容的密闭容器中,通入 和
和 ,发生反应:
,发生反应: ,下列说法不正确的是
,下列说法不正确的是
| A.当容器中 |
| B.当容器内的温度不再变化时,可判断反应已达到平衡 |
| C.保持其他条件不变,在反应过程中不断将氨液化并移去液氨,可提高合成氨的产率 |
| D.该反应可通过加入铁触媒做催化剂,降低反应所需的活化能,增加活化分子百分数,从而加快反应速率 |
用NH3催化还原NxOy可以消除氮氧化物的污染。已知:反应Ⅰ:4NH3(g)+6NO(g)  5N2(g)+6H2O(l) ΔH1
5N2(g)+6H2O(l) ΔH1
反应Ⅱ:2NO(g)+O2(g) 2NO2(g
2NO2(g ) ΔH2(且|ΔH1|=2|ΔH2|)
) ΔH2(且|ΔH1|=2|ΔH2|)
反应Ⅲ:4NH3(g)+6NO2(g) 5N2(g)+3O2(g)+6H2O(l) ΔH3
5N2(g)+3O2(g)+6H2O(l) ΔH3
反应Ⅰ和反应Ⅱ在不同温度时的平衡常数及其大小关系如下表:
(1)推测反应Ⅲ是________ 反应(填“吸热”或“放热”)
(2)相同条件下,反应Ⅰ在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率v(NO)=________ 。
②下列说法正确的是________ 。
a.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
b.增大压强能使反应速率加快,是因为增加了活化分子百分数
c.单位时间内H—O键与N—H键断裂的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已达到平衡
(3)一定条件下,反应Ⅱ达到平衡时体系中n(NO)∶n(O2)∶n(NO2)=2∶1∶2。在其他条件不变时,再充入NO2气体,分析NO2体积分数——φ(NO2)的变化情况:恒温恒压容器,φ(NO2)________ ;恒温恒容容器,φ(NO2)________ (填“变大”、“变小”或“不变”)。
(4)一定温度下,反应Ⅲ在容积可变的密闭容器中达到平衡,此时容积为3 L,c(N2)与反应时间t变化曲线X如图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z。则:

①变为曲线Y改变的条件是______________________________________ 。
变为曲线Z改变的条件是________________________________________ 。
②若t2时降低温度,t3时达到平衡,请在图中画出曲线X在t2~t4内c(N2)的变化曲线。____________________
反应Ⅱ:2NO(g)+O2(g)
 ) ΔH2(且|ΔH1|=2|ΔH2|)
) ΔH2(且|ΔH1|=2|ΔH2|)反应Ⅲ:4NH3(g)+6NO2(g)
反应Ⅰ和反应Ⅱ在不同温度时的平衡常数及其大小关系如下表:
| 温度/K | 反应Ⅰ | 反应Ⅱ | 已知:K2>K1>K′2>K′1 |
| 298 | K1 | K2 | |
| 398 | K′1 | K′2 |
(1)推测反应Ⅲ是
(2)相同条件下,反应Ⅰ在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①计算0~4分钟在A催化剂作用下,反应速率v(NO)=
②下列说法正确的是
a.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
b.增大压强能使反应速率加快,是因为增加了活化分子百分数
c.单位时间内H—O键与N—H键断裂的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已达到平衡
(3)一定条件下,反应Ⅱ达到平衡时体系中n(NO)∶n(O2)∶n(NO2)=2∶1∶2。在其他条件不变时,再充入NO2气体,分析NO2体积分数——φ(NO2)的变化情况:恒温恒压容器,φ(NO2)
(4)一定温度下,反应Ⅲ在容积可变的密闭容器中达到平衡,此时容积为3 L,c(N2)与反应时间t变化曲线X如图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z。则:

①变为曲线Y改变的条件是
变为曲线Z改变的条件是
②若t2时降低温度,t3时达到平衡,请在图中画出曲线X在t2~t4内c(N2)的变化曲线。
在绝热恒容的密闭容器中,通入0.1 mol N2和0.3 mol H2,发生反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0,下列说法不正确的是
| A.当容器中N2和H2物质的量浓度之比为1:3且保持不变时,可判断反应已达到平衡 |
| B.当容器内的温度不再变化时,可判断反应已达到平衡 |
| C.保持其他条件不变,在反应过程中,不断将氨液化并移去液氨,可提高合成氨的产率 |
| D.该反应可通过加入铁触媒做催化剂,从而降低反应所需的活化能,增加活化分子百分数,加快反应速率 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


