解答题-工业流程题 较难0.4 引用3 组卷407
HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧—水浸取法从HDS废催化剂(主要成分为MoS、NiS、V2O5、Al2O3)中提取贵重金属钒和钼,其工艺流程如图所示。
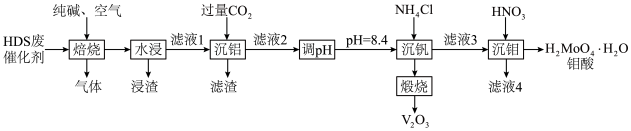
已知:I.焙烧时MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下NH4VO3易分解,分解产物常含N2和NH3两种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
请回答下列问题:
(1)流程的“气体”中含有二氧化碳,写出二氧化碳的一种用途:___________ 。
(2)请写出“焙烧”过程中Al2O3及MoS分别与纯碱反应的化学方程式:___________ ,___________ 。
(3)“浸渣”的成分为___________ (填化学式);“滤液2”中的成分除了Na2MoO4外,还含有___________ (填化学式)。
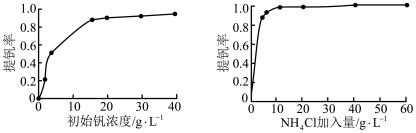
(4)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为___________ 、___________ 。
(5)在实际工业生产中,“沉钼”前要加入NH4HS除掉溶液中微量的Cu2+,反应Cu2++HS-=CuS+H+的平衡常数K=___________ 。
(6)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”中发生反应的化学方程式:___________ 。

已知:I.焙烧时MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下NH4VO3易分解,分解产物常含N2和NH3两种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
请回答下列问题:
(1)流程的“气体”中含有二氧化碳,写出二氧化碳的一种用途:
(2)请写出“焙烧”过程中Al2O3及MoS分别与纯碱反应的化学方程式:
(3)“浸渣”的成分为
(4)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为

(5)在实际工业生产中,“沉钼”前要加入NH4HS除掉溶液中微量的Cu2+,反应Cu2++HS-=CuS+H+的平衡常数K=
(6)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”中发生反应的化学方程式:
23-24高三上·四川遂宁·期中
类题推荐
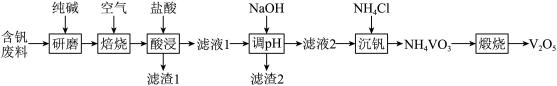
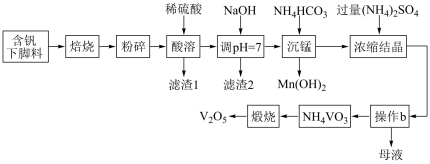
V2O5是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是V2O3,其中含铝、硅、铜、锰等的氧化物及油脂等杂质,一种以该下脚料为原料提取V2O5的工艺流程如下:
已知:ⅰ. V2O5 + 2H+ =2VO + H2O;VO
+ H2O;VO + H2O =VO
+ H2O =VO + 2H+。
+ 2H+。
ⅱ. 常温时,有关氢氧化物的溶度积常数如下表:
回答下列问题:
(1)“焙烧”可以除去油脂,还有一个作用是___________________________________ 。
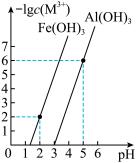
(2)“滤渣1”的主要成分是_____________ (写化学式),“调pH = 7”,析出沉淀后,滤液中c(Cu2+)∶c(Al3+) = _____________________ 。
(3)“沉锰”操作反应的离子方程式是_________________________________________ 。
(4)“浓缩结晶”时,需要加入过量(NH4)2SO4,其原因是_________________________ ;母液中溶质主要成分是_____________________ 。
(5)钒是一种应用广泛的金属,工业上可用金属钙还原高纯度的V2O5制得金属钒。请写出钙热还原法制钒的化学反应方程式______________________________________ 。

已知:ⅰ. V2O5 + 2H+ =2VO
ⅱ. 常温时,有关氢氧化物的溶度积常数如下表:
氢氧化物 | Mn(OH)2 | Cu(OH)2 | Al(OH)3 |
Ksp | 4.00×10−14 | 2.20×10−20 | 1.90×10−33 |
(1)“焙烧”可以除去油脂,还有一个作用是
(2)“滤渣1”的主要成分是
(3)“沉锰”操作反应的离子方程式是
(4)“浓缩结晶”时,需要加入过量(NH4)2SO4,其原因是
(5)钒是一种应用广泛的金属,工业上可用金属钙还原高纯度的V2O5制得金属钒。请写出钙热还原法制钒的化学反应方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网