解答题-实验探究题 适中0.65 引用2 组卷101
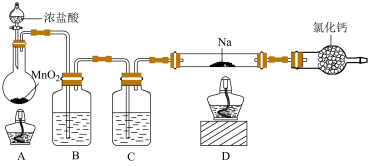
某同学利用如图所示装置(夹持装置已省略)制备氯气并探究其部分性质。
请回答下列问题:
(1)装置A中发生反应的离子方程式为___________ ;装置B的作用为___________ ;装置C中的试剂为___________ 。
(2)实验开始时,先点燃A处酒精灯,待观察到D中硬质玻璃管内充满黄绿色气体时,再点燃D处酒精灯,目的是___________ 。
(3)装置D中发生反应的化学方程式为___________ 。
(4)将装置E中出来的尾气通入滴有酚酞的NaOH溶液中,发生反应的离子方程式为___________ ;观察到溶液红色褪去,甲同学认为是反应生成了漂白性物质导致的,乙同学则认为是NOH被完全消耗导致的。指导老师做了如下实验对甲、乙同学的猜想进行验证:取适量反应后的溶液于试管1中,加入过量___________ ,溶液无明显现象,证明乙同学猜想错误;另取适量原反应后的溶液于试管2中,加入适量___________ ,溶液变红,证明甲同学猜想正确。(供选择的试剂:稀硫酸、NaOH溶液、紫色石蕊溶液、无色酚酞溶液、氯水)

请回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)实验开始时,先点燃A处酒精灯,待观察到D中硬质玻璃管内充满黄绿色气体时,再点燃D处酒精灯,目的是
(3)装置D中发生反应的化学方程式为
(4)将装置E中出来的尾气通入滴有酚酞的NaOH溶液中,发生反应的离子方程式为
23-24高一上·云南楚雄·期中
类题推荐
化学小组对Na在CO2气体中燃烧的产物进行了实验探究。
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O和Na2CO3
【查阅资料】①N2的化学性质较稳定,通常情况下不与其他物质反应;
②PdCl2溶液能与CO反应生成黑色的金属钯,同时生成强酸性物质;
③将酚酞溶液分别滴入BaCl2、NaCl、NaOH、Na2CO3四种溶液中的现象如下:
【实验1】化学小组在老师的指导下设计了如图所示装置(部分夹持仪器已略去):

步骤一:向甲装置的玻璃管中通入适量N2.
步骤二:停止通入N2,点燃酒精灯,再通入CO2气体,Na剧烈燃烧,生成黑色和白色两种固体;装置丁中有黑色沉淀产生;装置戊中溶液变浑浊。
(1)步骤一中通入N2的目的是______ ,乙装置的作用是______ 。
(2)根据步骤二的实验现象推理可知,Na与CO2反应的产物一定有______ (填化学式)。
(3)写出装置丁中反应的化学方程式:______ 。
【实验2】为了进一步探究步骤二中所得白色固体的组成,兴趣小组同学继续进行如下实验:取实验1步骤二中的白色固体于试管中,加入适量水后振荡,固体完全溶解,滴入几滴酚酞溶液,溶液由无色变为红色。
(4)有同学认为,根据实验2中溶液颜色的变化可以证明白色固体为Na2O,其推理的依据是______ 。
(5)另有同学认为实验2中的现象并不能证明白色固体一定是Na2O,也可能是Na2CO3,设计了如下实验方案进行探究,请结合题给信息,完善验证该实验方案:
取实验1步骤二中的白色固体于试管中,加适量水溶解,滴加______ (填化学式)至不再产生沉淀,过滤,向滤液中滴加______ ,无明显现象,则证明该白色固体中必定含有Na2CO3,且不含Na2O。
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O和Na2CO3
【查阅资料】①N2的化学性质较稳定,通常情况下不与其他物质反应;
②PdCl2溶液能与CO反应生成黑色的金属钯,同时生成强酸性物质;
③将酚酞溶液分别滴入BaCl2、NaCl、NaOH、Na2CO3四种溶液中的现象如下:
| 溶液 | BaCl2 | NaCl | NaOH | Na2CO3 |
| 现象 | 无变化 | 无变化 | 溶液变为红色 | 溶液变为红色 |

步骤一:向甲装置的玻璃管中通入适量N2.
步骤二:停止通入N2,点燃酒精灯,再通入CO2气体,Na剧烈燃烧,生成黑色和白色两种固体;装置丁中有黑色沉淀产生;装置戊中溶液变浑浊。
(1)步骤一中通入N2的目的是
(2)根据步骤二的实验现象推理可知,Na与CO2反应的产物一定有
(3)写出装置丁中反应的化学方程式:
【实验2】为了进一步探究步骤二中所得白色固体的组成,兴趣小组同学继续进行如下实验:取实验1步骤二中的白色固体于试管中,加入适量水后振荡,固体完全溶解,滴入几滴酚酞溶液,溶液由无色变为红色。
(4)有同学认为,根据实验2中溶液颜色的变化可以证明白色固体为Na2O,其推理的依据是
(5)另有同学认为实验2中的现象并不能证明白色固体一定是Na2O,也可能是Na2CO3,设计了如下实验方案进行探究,请结合题给信息,完善验证该实验方案:
取实验1步骤二中的白色固体于试管中,加适量水溶解,滴加
某化学兴趣小组对 与
与 的产物进行了探究.
的产物进行了探究.
同学们经过讨论,提出了如下猜想:
猜想1:产物为 和
和
猜想2:产物为
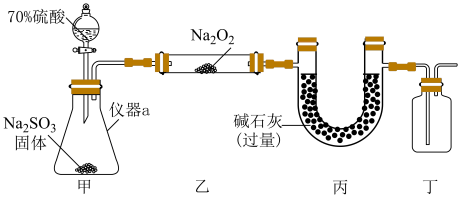
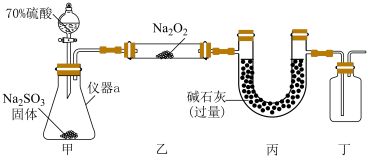
甲同学设计如图所示实验装置(夹持装置已省略)制备 并进行实验探究,请回答下列问题:
并进行实验探究,请回答下列问题:__________ ;打开分液漏斗活塞,装置甲中发生反应的离子方程式为__________ ;使用70%的硫酸而不用98%的硫酸的原因是__________ .
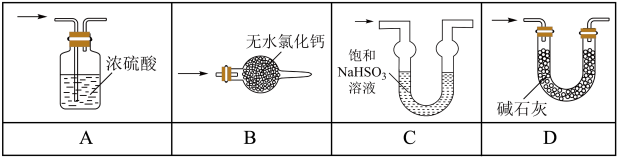
(2)①甲同学用带火星的木条检验出丁中收集的气体为氧气,该同学认为猜想1正确,乙同学分析装置后推翻了甲同学的结论,乙同学的理由可能是__________ ,乙同学对实验装置进行了改进,在装置甲和装置乙之间添加了装置戊,装置戊可能是__________ (填标号).
②改进实验装置后,丙同学在乙处硬质玻璃管内淡黄色固体全部变成白色后,取适量反应后的白色固体a于试管i中,加入适量的稀硫酸,有气泡产生,将产生的气体通入适量酸性高锰酸钾溶液b中,溶液b褪色,说明固体a中含有__________ (填化学式),溶液b褪色的离子方程式为__________ ;另取适量固体a于试管ii中,加入足量的稀盐酸酸化,充分反应后,加入适量的 溶液,观察到有白色沉淀产生,该白色沉淀为
溶液,观察到有白色沉淀产生,该白色沉淀为__________ (填化学式)。
实验结论: 与
与 在常温时就能发生化学反应,生成
在常温时就能发生化学反应,生成__________ (填化学式)和 .
.
同学们经过讨论,提出了如下猜想:
猜想1:产物为
猜想2:产物为
甲同学设计如图所示实验装置(夹持装置已省略)制备
(2)①甲同学用带火星的木条检验出丁中收集的气体为氧气,该同学认为猜想1正确,乙同学分析装置后推翻了甲同学的结论,乙同学的理由可能是
|
|
|
|
A | B | C | D |
实验结论:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网