解答题-工业流程题 适中0.65 引用1 组卷147
NCM是三元锂电池最重要的前驱体材料,一种以镍钴杂料(主要成分为 、
、 、
、 ,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
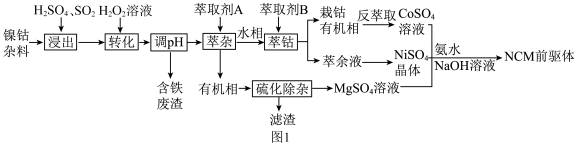
回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为___________ 。
(2)为提高“浸出”效率,可采取的措施有___________ (写出一条即可);“浸出”过程中 的作用是
的作用是___________ (用离子方程式表示)。
(3)常温下,若“转化”后的溶液中 浓度为
浓度为 ,在“调
,在“调 ”过程中,当
”过程中,当 调节到2.2时,开始出现
调节到2.2时,开始出现 沉淀,若要使
沉淀,若要使 完全沉淀,则调节溶液
完全沉淀,则调节溶液 最小为
最小为___________ [已知:当c(Fe3+)≤1×10-5mol/L时,认为 沉淀完全]
沉淀完全]
(4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。
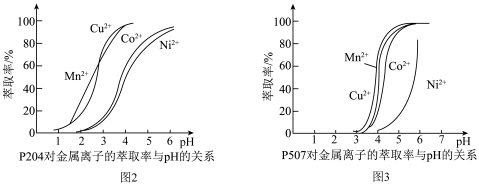
①萃取剂A是___________ (填“P204”或“P507”,下同),萃取剂B是___________ 。
②进行“萃钴”操作前,需对水相调pH至___________ (填标号),以达到最佳萃取 的效果。
的效果。
a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取 的原理为2HR(有机相)
的原理为2HR(有机相) (水相)
(水相) (有机相)
(有机相) (水相),则反萃取操作中可向载钴有机相中加入
(水相),则反萃取操作中可向载钴有机相中加入___________ (填试剂名称)得到含 的溶液;一定条件下,萃取平衡时,溶液中
的溶液;一定条件下,萃取平衡时,溶液中 ,则
,则 的萃取率为
的萃取率为___________ 。
(5)一种NiAs晶体结构如图4所示。
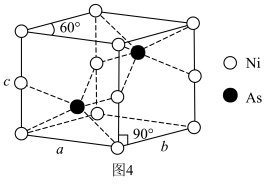
通过X射线光谱测算出该晶胞参数为 ,
, ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶体密度为
,则该晶体密度为___________ (填含m、n和 的表达式)
的表达式) 。
。

回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为
(2)为提高“浸出”效率,可采取的措施有
(3)常温下,若“转化”后的溶液中
(4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。

①萃取剂A是
②进行“萃钴”操作前,需对水相调pH至
a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取
(5)一种NiAs晶体结构如图4所示。

通过X射线光谱测算出该晶胞参数为
23-24高三上·云南楚雄·期中
类题推荐
以Al2O3为载体的钴钼废催化剂中含CoS、MoS2及少量Fe、Si、Ca等元素的物质,经系列处理可制取CoCO3、(NH4)2MoO4,工艺流程如图所示: 。
。
②常温下,Ksp(CoCO3)=a,Ksp(Co(OH)2)=b,Kb(NH3·H2O)=c。
(1)“酸浸”时,投料完成后,保持酸浸温度不变,以一定速率搅拌反应,能提高钴、钼元素浸出率的方法还有___________ 。(任写一种)
(2)有关沉淀数据如下表(“完全沉淀”时溶液中金属离子浓度≤1.0×10-5mol·L-1)
“滤渣2”的主要成分为Fe(OH)3和Al(OH)3,“调pH”时,若浸取液中c(Co2+)=0.1mol·L-1,则需调节溶液pH的范围是___________ (加入物质对溶液体积的变化忽略不计)。
(3)“沉钴”时,其离子方程式为___________ 。“沉钴”过程中为防止CoCO3转化为Co(OH)2,需控制溶液pH,转化时存在CoCO3(s)+2NH3·H2O(aq) Co(OH)2(s)+
Co(OH)2(s)+ (aq)+2
(aq)+2 (aq),该反应的平衡常数K=
(aq),该反应的平衡常数K=___________ (用含a、b、c的表达式作答)。
(4)“萃取”的反应原理为2R3N(叔胺)+2H+ +
 (R3NH)2MoO4,通过反萃取法使有机相中的Mo元素回到水相,需加反萃取剂氨水,而不使用NaOH的原因是
(R3NH)2MoO4,通过反萃取法使有机相中的Mo元素回到水相,需加反萃取剂氨水,而不使用NaOH的原因是___________ 。
(5)制MoS2用(NH4)2MoO4晶体先制备硫代钼酸铵[(NH4)2MoS4],再将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和单质硫。其中NH3、H2S和单质硫的物质的量之比为8:4:1,所得硫单质的分子式为___________ 。

②常温下,Ksp(CoCO3)=a,Ksp(Co(OH)2)=b,Kb(NH3·H2O)=c。
(1)“酸浸”时,投料完成后,保持酸浸温度不变,以一定速率搅拌反应,能提高钴、钼元素浸出率的方法还有
(2)有关沉淀数据如下表(“完全沉淀”时溶液中金属离子浓度≤1.0×10-5mol·L-1)
| 沉淀 | Al(OH)3 | Fe(OH)3 | Co(OH)2 |
| 恰好完全沉淀时pH | 5.2 | 2.8 | 9.4 |
(3)“沉钴”时,其离子方程式为
(4)“萃取”的反应原理为2R3N(叔胺)+2H+ +
(5)制MoS2用(NH4)2MoO4晶体先制备硫代钼酸铵[(NH4)2MoS4],再将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和单质硫。其中NH3、H2S和单质硫的物质的量之比为8:4:1,所得硫单质的分子式为
三氧化二镍(Ni2O3)是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含Ni、Al、Fe的氧化物,SiO2、C等)制备Ni2O3的工艺流程如下所示:

已知:①在该实验条件下NaClO3、Fe3+不能氧化Ni2+。
②常温下,溶液中金属离子形成氢氧化物沉淀的如下表所示:
③萃取的原理为。Ni2+(水相) + 2HR(有机相) ⇌NiR2(有机相)+ 2H+(水相) 回答下列问题:
(1)“预处理时,可以用___________ (填化学式)溶液除去废料表面的油脂油污。
(2)“浸出时,提高浸出效率可采取的措施有___________ (任写一种)。滤渣1的主要成分是___________ 。
(3)“氧化时,加入NaClO3发生反应的离子方程式为___________ ,目的是___________ 。
(4)若常温下,“调pH时,溶液中Ni2+浓度为0.1mol/L,为使Al3+等杂质离子沉淀完全( ),经过计算,需控制溶液的pH范围是
),经过计算,需控制溶液的pH范围是___________ 。
(5)“萃取时,操作若在实验室进行,需要用到的主要玻璃仪器有___________ 、烧杯。请利用化学平衡原理解释该流程中用H2SO4反萃取的原理___________ 。

已知:①在该实验条件下NaClO3、Fe3+不能氧化Ni2+。
②常温下,溶液中金属离子形成氢氧化物沉淀的如下表所示:
| 离子pH | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 完全沉淀pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“预处理时,可以用
(2)“浸出时,提高浸出效率可采取的措施有
(3)“氧化时,加入NaClO3发生反应的离子方程式为
(4)若常温下,“调pH时,溶液中Ni2+浓度为0.1mol/L,为使Al3+等杂质离子沉淀完全(
(5)“萃取时,操作若在实验室进行,需要用到的主要玻璃仪器有
三氧化二镍( )是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含Ni、Al、Fe的氧化物,
)是重要的电子元件和蓄电池材料,工业上利用含镍废料(主要含Ni、Al、Fe的氧化物, ,C等)制备
,C等)制备 的工艺流程如下所示:
的工艺流程如下所示:
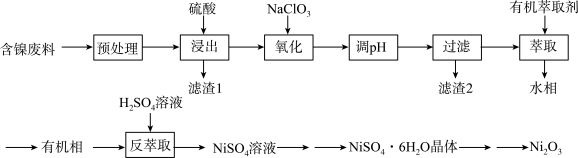
已知:①在该实验条件下 、
、 不能氧化
不能氧化 。
。
②常温下,溶液中0.010 mol/L金属离子形成氢氧化物沉淀的pH如下表所示:
③萃取的原理为 (水相)
(水相) (有机相)
(有机相) (有机相)
(有机相) (水相)
(水相)
回答下列问题:
(1)“预处理”时,可以用_______ (填化学式)溶液除去废料表面的油脂油污。
(2)“浸出”时,提高浸出效率可采取的措施有_______ (任写一种)。
(3)“氧化”时,加入 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)若常温下,“调pH”时,溶液中 浓度为0.1 mol/L,为使
浓度为0.1 mol/L,为使 等杂质离子沉淀完全(
等杂质离子沉淀完全( mol/L),经过计算,需控制溶液的pH范围是
mol/L),经过计算,需控制溶液的pH范围是_______ 。
(5)“萃取”时,操作若在实验室进行,需要用到的主要玻璃仪器有_______ 、烧杯。请利用化学平衡原理解释该流程中用 反萃取的原理
反萃取的原理_______ 。

已知:①在该实验条件下
②常温下,溶液中0.010 mol/L金属离子形成氢氧化物沉淀的pH如下表所示:
离子 pH | ||||
| 开始沉淀pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 完全沉淀pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
(1)“预处理”时,可以用
(2)“浸出”时,提高浸出效率可采取的措施有
(3)“氧化”时,加入
(4)若常温下,“调pH”时,溶液中
(5)“萃取”时,操作若在实验室进行,需要用到的主要玻璃仪器有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


