解答题-原理综合题 适中0.65 引用1 组卷50
工业合成氨是人类科学技术的一项重大突破,其原理为N2(g)+3H2(g) 2NH3(g) △H<0生产示意图如图:
2NH3(g) △H<0生产示意图如图:
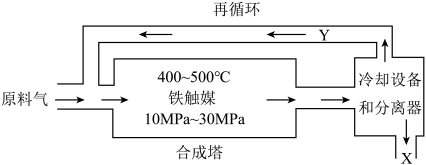
(1)下列有关合成氨工业的说法正确的是________ 。
(2)循环利用的Y是________ ,目的是________ 。
(3)合成氨反应中,某时刻改变条件速率变化如图:

图I中t0时刻改变的条件是________ ,图II中t0时刻改变的条件是________ 。
(4)在合成氨工业中,既能加快反应速率,又能增大氢气转化率采取的措施是________ 。
A.增加N2
B.移走NH3
C.升高温度
D.恒温恒容,充入惰性气体Ar使压强增大
E.压缩体积
(5)氮的固定和氮的循环是几百年来科学家一直研究的课题。如表列举了不同温度下大气固氮和工业固氮的部分K值。
①分析数据可知:①在400℃下模拟工业固氮,某时刻c(N2)=c(H2)=c(NH3)=1mol•L-1,此时v正________ v逆(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是________ 。

(1)下列有关合成氨工业的说法正确的是
| A.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
| C.合成氨厂一般采用的压强为10MPa~30MPa,因为该压强下铁触媒的活性最高 |
| D.N2的量越多,H2的转化率越大,因此,充入的N2越多越有利于NH3的合成 |
(2)循环利用的Y是
(3)合成氨反应中,某时刻改变条件速率变化如图:

图I中t0时刻改变的条件是
(4)在合成氨工业中,既能加快反应速率,又能增大氢气转化率采取的措施是
A.增加N2
B.移走NH3
C.升高温度
D.恒温恒容,充入惰性气体Ar使压强增大
E.压缩体积
(5)氮的固定和氮的循环是几百年来科学家一直研究的课题。如表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮N2(g)+O2(g) | 工业固氮N2(g)+3H2(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②人类不适合大规模模拟大气固氮的原因是
23-24高二上·四川南充·阶段练习
类题推荐
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖。工业合成氨生产示意图如图所示。

(1)下列有关合成氨工业的说法正确的是_________
(2)循环利用的Y是氮气和氢气,目的是__________________ 。
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有_________ (填编号)。
①使用催化剂 ②恒温恒容,增大原料气 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体 使压强增大
使压强增大
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分 值。
值。
分析数据可知:
①在 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻 ,此时
,此时
_________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是__________________ 。
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下。
的过程如下。
已知: 。
。
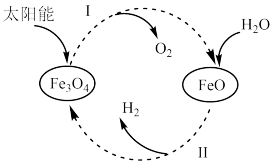
过程Ⅰ:
过程Ⅱ:……
过程Ⅱ的热化学方程式为_________ 。

(1)下列有关合成氨工业的说法正确的是_________
| A.工业合成氨的反应是熵减小的放热反应,在低温或常温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
| C.合成氨厂一般采用的压强为 |
| D. |
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂 ②恒温恒容,增大原料气
④升高温度 ⑤恒温恒容,充入惰性气体
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分
| 反应 | 大气固氮 | 工业固氮 | |||
| 温度 | 27 | 2000 | 25 | 400 | 450 |
| 0.1 | 0.507 | 0.152 | |||
①在
②人类不适合大规模模拟大气固氮的原因是
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解
已知:

过程Ⅰ:
过程Ⅱ:……
过程Ⅱ的热化学方程式为
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖。工业合成氨生产示意图如图所示。
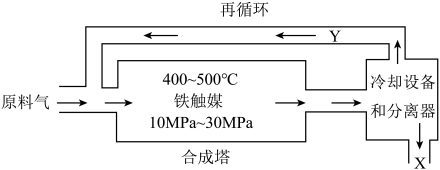
(1)下列有关合成氨工业的说法正确的是___________
(2)循环利用的Y是氮气和氢气,目的是___________ 。
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有___________ (填编号)。
①使用催化剂 ②恒温恒容,增大原料气 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体 使压强增大
使压强增大
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分 值。
值。
分析数据可知:
①在 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻 ,此时v正
,此时v正___________ v逆(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是___________ 。
(5)哈伯1908年发表的文献中写到,在高温下,铁和铂都能作为使气态氨分解成为氢气、氮气的催化剂,下面是他做过的实验中的两组(条件都为901℃和3039.75 kPa)。
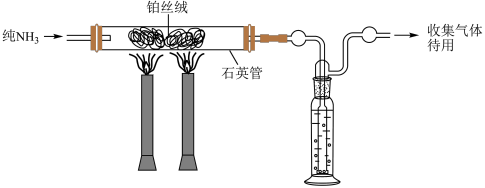
①使纯氨气通过白炽的铂丝,剩余的氨用浓硫酸洗涤除去。然后使气态混合物在相同条件下通过铁催化剂,出来的气体再缓缓通过20mL盐酸除去氨气。用气量计测得标准状况下剩余干燥气体的体积为2.02L。盐酸溶液用KOH溶液滴定,最终计算得到通入盐酸前氨气为1.86×10-4mol。
计算回答:在901℃下,N2 (g)+ 3H2 (g)
(g) 2NH3(g)的Kp=
2NH3(g)的Kp=___________ kPa-2。(保留一位有效数字)
②使纯氨气直接通过同一铁催化剂,出来的气体同样缓缓通入20mL盐酸,用气量计测得标准状况下剩余干燥气体的体积为1.82L。同理可以滴定后计算出通入盐酸前氨气的量,进而计算出Kp。在操作、计算误差合理的范围内,①、②得到的Kp基本相等。这对你有何启发?___________ 。

(1)下列有关合成氨工业的说法正确的是___________
| A.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
| C.合成氨厂一般采用的压强为 |
| D. |
(2)循环利用的Y是氮气和氢气,目的是
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂 ②恒温恒容,增大原料气
④升高温度 ⑤恒温恒容,充入惰性气体
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分
| 反应 | 大气固氮 | 工业固氮 | |||
| 温度 | 27 | 2000 | 25 | 400 | 450 |
| 0.1 | 0.507 | 0.152 | |||
①在
②人类不适合大规模模拟大气固氮的原因是
(5)哈伯1908年发表的文献中写到,在高温下,铁和铂都能作为使气态氨分解成为氢气、氮气的催化剂,下面是他做过的实验中的两组(条件都为901℃和3039.75 kPa)。

①使纯氨气通过白炽的铂丝,剩余的氨用浓硫酸洗涤除去。然后使气态混合物在相同条件下通过铁催化剂,出来的气体再缓缓通过20mL盐酸除去氨气。用气量计测得标准状况下剩余干燥气体的体积为2.02L。盐酸溶液用KOH溶液滴定,最终计算得到通入盐酸前氨气为1.86×10-4mol。
计算回答:在901℃下,N2 (g)+ 3H2
②使纯氨气直接通过同一铁催化剂,出来的气体同样缓缓通入20mL盐酸,用气量计测得标准状况下剩余干燥气体的体积为1.82L。同理可以滴定后计算出通入盐酸前氨气的量,进而计算出Kp。在操作、计算误差合理的范围内,①、②得到的Kp基本相等。这对你有何启发?
氮的固定以及利用氨合成其他含氮化合物是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
①分析数据可知:大气固氮反应属于____________ (填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因______________________________________ 。
③在500 ℃、2.02×107 Pa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量________ (填“大于”、“小于”或“等于”)92.4 kJ。
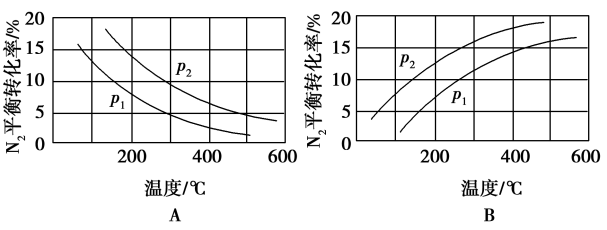
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,如图所示的图示中,正确的是___________ (填“A”或“B”);比较p1、p2的大小关系:___________ 。
(3)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生工业合成氨反应,达到平衡状态时,测得气体总物质的量为2.8 mol。
①达平衡时,H2的转化率α1=_____________ 。
②已知平衡时,容器压强为8MPa,则平衡常数Kp=_________________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③为提高H2的转化率,实际生产中宜采取的措施有______________ (填字母)。
A.降低温度 B.最适合催化剂活性的适当高温 C.适当增大压强
D.减小压强 E.循环利用和不断补充氮气 F.及时移出氨
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮 N2(g)+O2(g)  2NO(g) 2NO(g) | 工业固氮 N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1 2NH3(g) ΔH=-92.4 kJ·mol-1 | |||
| 温度/℃ | 27 | 2 000 | 25 | 400 | 450 |
| K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因
③在500 ℃、2.02×107 Pa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,如图所示的图示中,正确的是
(3)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生工业合成氨反应,达到平衡状态时,测得气体总物质的量为2.8 mol。
①达平衡时,H2的转化率α1=
②已知平衡时,容器压强为8MPa,则平衡常数Kp=
③为提高H2的转化率,实际生产中宜采取的措施有
A.降低温度 B.最适合催化剂活性的适当高温 C.适当增大压强
D.减小压强 E.循环利用和不断补充氮气 F.及时移出氨
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


