单选题 较易0.85 引用2 组卷121
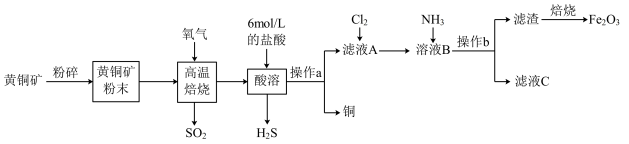
工业上用生物法处理 的原理如下:
的原理如下:
反应1:
反应2:
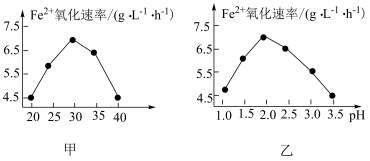
以硫杆菌作催化剂时,反应温度及溶液 对
对 氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
反应1:
反应2:
以硫杆菌作催化剂时,反应温度及溶液

| A.反应1的条件下,还原性: |
| B.当反应温度过高时, |
| C.由图甲和图乙可得出结论:使用硫杆菌作催化剂的最佳条件为 |
| D.当反应1中转移 |
23-24高二上·江西赣州·期中
类题推荐  被硫杆菌催化氧化的反应为
被硫杆菌催化氧化的反应为 。硫杆菌存在时
。硫杆菌存在时 被氧化的速率与温度的关系如图所示。下列有关说法错误的是
被氧化的速率与温度的关系如图所示。下列有关说法错误的是

工业上用生物法处理H2S的原理如下:
反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2 2Fe(SO4)3+2H2O
2Fe(SO4)3+2H2O
以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

反应1:H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
反应2:4Fe2SO4+2H2SO4+O2
以硫杆菌作催化剂时,反应温度及溶液pH对Fe2+氧化速率的影响分别如图1、图2所示,下列说法不正确的是

| A.上述总反应方程式为:2H2S+O2=2S↓+2H2O,Fe2(SO4)3是该反应的催化剂 |
| B.当反应温度过高时,Fe2+氧化速率下降的原因可能是硫杆菌失去活性 |
| C.由图-1、图-2可得出结论:使用硫杆菌作催化剂的最佳条件为30℃、pH=2.0 |
| D.当反应1中转移0.1mol电子时,反应1中消耗的H2S在标准状况下的体积为2.24L |

| A.硫杆菌作催化剂 |
| B. |
| C. |
| D.硫杆菌可能在40℃时失去生物活性 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网