单选题 较易0.85 引用3 组卷252
一定条件下N2(g)、O2(g)反应生成NO(g)的能量关系如图所示,下列说法错误的是
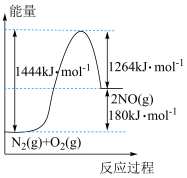

| A. |
| B.该反应中反应物分子的每次碰撞都为有效碰撞 |
| C.正反应的活化能大于逆反应的活化能 |
| D.使用催化剂可增加单位时间内NO的产量 |
23-24高二上·甘肃武威·期中
类题推荐
下列关于可逆反应2SO2(g) + O2(g)  2SO3 (g) △H< 0 的说法中正确的是
2SO3 (g) △H< 0 的说法中正确的是
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内活化分子百分数增多,反应速率加快 |
| C.升高反应体系温度,可使单位体积内活化分子增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加,反应速率加快 |
下列关于碰撞理论的说法中错误的是
| A.反应物分子只有发生有效碰撞才能发生化学反应 |
| B.催化剂能够降低反应的活化能,使得更多的分子成为活化分子 |
| C.增大浓度能使单位时间内分子的有效碰撞次数增加,反应速率加快 |
| D.增大压强能够提高活化分子的百分率,提高单位时间内分子有效碰撞次数 |
反应:2N2O5(g)=4NO2(g)+O2(g)的历程如下:
第一步:N2O5(g) NO2(g)+NO3(g) △H1
NO2(g)+NO3(g) △H1
第二步:NO2(g)+NO3(g) NO(g)+NO2(g)+O2(g) △H2(慢反应)
NO(g)+NO2(g)+O2(g) △H2(慢反应)
第三步:NO(g)+NO3(g)=2NO2(g) △H3(快反应)
下列说法错误的是
第一步:N2O5(g)
第二步:NO2(g)+NO3(g)
第三步:NO(g)+NO3(g)=2NO2(g) △H3(快反应)
下列说法错误的是
| A.其他条件不变,使用催化剂可以增大第一步中NO2的平衡产量 |
| B.第二步NO2和NO3的碰撞只有部分有效 |
| C.反应2N2O5(g) |
| D.第二步反应的活化能大于第三步反应的活化能 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


