单选题 较易0.85 引用1 组卷236
标准状况下,气态反应物和生成物的相对能量与反应历程示意图如下。已知: 和
和 的相对能量为0,下列说法正确的是
的相对能量为0,下列说法正确的是
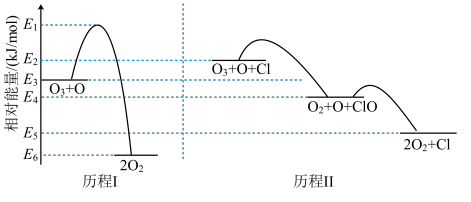

| A.历程Ⅰ总反应的 |
| B.可计算Cl-Cl键能为: |
| C.相同条件下, |
| D.历程Ⅱ中速率最快的一步反应的热化学方程式为: |
23-24高二上·辽宁大连·期中
知识点:根据△H=生成物的总能量之和-反应物的总能量之和进行计算活化能及其对反应速率的影响催化剂对化学反应速率的影响转化率的相关计算及判断 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下(已知O2和Cl2的相对能量为0),下列说法错误的是

| A. |
| B.可计算 |
| C.相同条件下,O3的平衡转化率:历程Ⅱ=历程Ⅰ |
| D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:ClO(g)+O(g)=O2(g)+Cl(g) ΔH=(E4-E5)kJ∙mol−1 |
标准状况下,气态反应物和生成物的相对能量与反应历程示意图如下,已知: 和
和 的相对能量为0。下列说法错误的是
的相对能量为0。下列说法错误的是
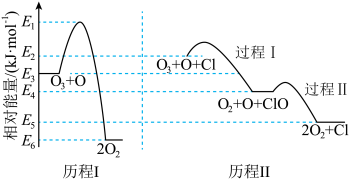

| A.相同条件下, |
| B.可计算 |
| C.由图可知 |
| D.历程Ⅱ反应的快慢取决于过程Ⅰ反应的快慢 |
标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下(已知O2(g)和Cl2(g)的相对能量为0),下列说法正确的是


| A.历程II中Cl起催化作用,并且E6−E3>E5−E2 |
| B.可计算Cl−Cl键能为(E2−E3) kJ∙mol−1 |
| C.历程I、历程II中速率最快的一步反应的热化学方程式 |
| D.相同条件下, |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


