单选题 适中0.65 引用1 组卷222
黄铵铁矾是硫酸体系中除铁的常用试剂,化学式可表示为 (其中铁为+3价),摩尔质量为480g/mol。依据下列实验和数据可确定黄铵铁矾的化学式。
(其中铁为+3价),摩尔质量为480g/mol。依据下列实验和数据可确定黄铵铁矾的化学式。
Ⅰ.称取黄铵铁矾2.400g,加入足量NaOH溶液充分反应后过滤,向滤液中加入是量盐酸酸化的BaCl2溶液,得到沉淀2.330g。
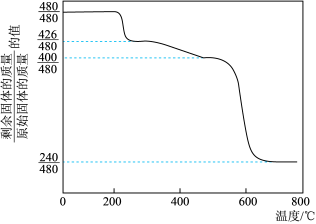
Ⅱ.对黄铵铁矾样品进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300℃前分解释放的物质为H2O,300~575℃之间只有NH3和H2O放出,670℃以上得到的是纯净的红棕色粉末)。下列说法中不正确的是
Ⅰ.称取黄铵铁矾2.400g,加入足量NaOH溶液充分反应后过滤,向滤液中加入是量盐酸酸化的BaCl2溶液,得到沉淀2.330g。
Ⅱ.对黄铵铁矾样品进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300℃前分解释放的物质为H2O,300~575℃之间只有NH3和H2O放出,670℃以上得到的是纯净的红棕色粉末)。下列说法中不正确的是

| A.根据实验可知,z=2 |
| B.300~575℃之间完全释放出气体后,残留固体中估计存在Fe、O、S三种元素 |
| C.2.400g样品中铁元素的质量为0.84g |
| D.根据计算可得,x=2,w=6 |
23-24高一上·江苏南通·期中
类题推荐
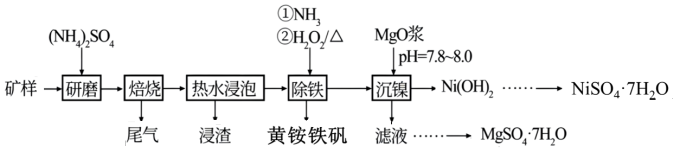
工业上以红土镍矿(主要成分Mg3Si2O5(OH)4、Fe2MgO4、NiO、FeO、Fe2O3)为原料,采用硫酸铵焙烧法选择性提取镍及其化合物,并回收副产物黄铵铁矾。工艺流程如下图所示:
已知:
①在焙烧过程中Mg3Si2O5(OH)4和Fe2MgO4转化为(NH4)2Mg2(SO4)3、(NH4)3Fe(SO4)3及SiO2 ;
②加热情况下,Fe3+可水解生成一种难溶于水的黄色固体FeO(OH);
③常温下,NiSO4易溶于水,NiOOH不溶于水。
(1)在该工艺流程中为了加快化学反应速率而采取的主要措施有_______ (至少回答两项)
(2)经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与(NH4)2SO4反应生成Fe2(SO4)3,该反应的化学方程式为_______ ,“浸渣"的主要成分除铁的氧化物外还有_______ (填化学式)。
(3)“除铁”和“沉镍"时需将Fe3+、Ni2+转化为沉淀。已知溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
若“沉镍"时pH调为7.8,则滤液中Ni2+浓度约为_______ mol/L。
(4)流程中由Ni(OH)2沉淀得到NiSO4·7H2O晶体的操作是_______ ;NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式是_______ 。
(5)依据下列实验和数据可确定黄铵铁矾【化学式可表示为(NH4)xFey(SO4)z(OH)m,摩尔质量为480g/mol】的化学式。
①称取黄铵铁矾2.400 g,加入足量NaOH溶液充分反应后过滤,向滤液中加入足量盐酸酸化,再加入足量的BaCl2溶液,得到沉淀2.330 g。
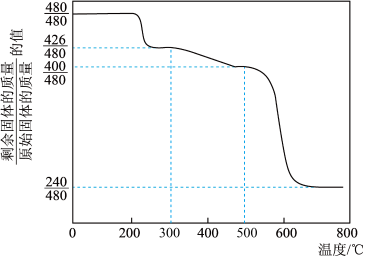
②Mim Ristic等曾对黄铵铁矾进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300 ℃前分解释放的物质为H2O,300~575 ℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670 ℃以上得到的是纯净的红棕色粉末)。
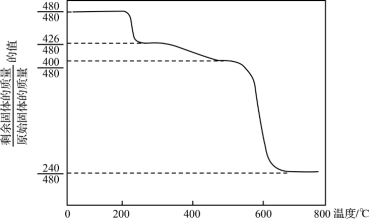
根据以上实验及图中数据确定黄铵铁矾的化学式_______ 。

已知:
①在焙烧过程中Mg3Si2O5(OH)4和Fe2MgO4转化为(NH4)2Mg2(SO4)3、(NH4)3Fe(SO4)3及SiO2 ;
②加热情况下,Fe3+可水解生成一种难溶于水的黄色固体FeO(OH);
③常温下,NiSO4易溶于水,NiOOH不溶于水。
(1)在该工艺流程中为了加快化学反应速率而采取的主要措施有
(2)经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与(NH4)2SO4反应生成Fe2(SO4)3,该反应的化学方程式为
(3)“除铁”和“沉镍"时需将Fe3+、Ni2+转化为沉淀。已知溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 沉淀物 | 黄铵铁矾 | Fe(OH)3 | Ni(OH)2 |
| 开始沉淀时的pH | 1.3 | 2.7 | 7.1 |
| 沉淀完全(c=1×10-5 mol/L)时的pH | 2.3 | 3.7 | 9.2 |
若“沉镍"时pH调为7.8,则滤液中Ni2+浓度约为
(4)流程中由Ni(OH)2沉淀得到NiSO4·7H2O晶体的操作是
(5)依据下列实验和数据可确定黄铵铁矾【化学式可表示为(NH4)xFey(SO4)z(OH)m,摩尔质量为480g/mol】的化学式。
①称取黄铵铁矾2.400 g,加入足量NaOH溶液充分反应后过滤,向滤液中加入足量盐酸酸化,再加入足量的BaCl2溶液,得到沉淀2.330 g。
②Mim Ristic等曾对黄铵铁矾进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300 ℃前分解释放的物质为H2O,300~575 ℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670 ℃以上得到的是纯净的红棕色粉末)。

根据以上实验及图中数据确定黄铵铁矾的化学式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网