填空题 适中0.65 引用1 组卷42
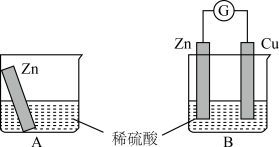
I.某兴趣小组为探究原电池工作原理,利用金属Zn与稀H2SO4反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作_______ (填“正”或“负”)极,Zn电极上的电极反应式为_______ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为_______ ;“离子导体”中H+离子的移动方向可描述为_______ 。
(3)从反应速率的角度上看,可以观察到A中反应比B中_______ (填“快”或“慢”)
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为_______ 。
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据填空:
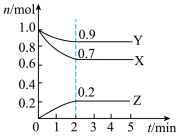
(5)该反应的化学方程式为_______ ;
(6)反应开始至2min末,以气体X表示的平均反应速率为_______ ;
(7)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是_______ 。
①混合气体的压强不再变化 ②混合气体的密度不再变化 ③X的百分含量不再变化 ④混合气体的平均相对分子质量不再变化 ⑤v(X):v(Y)=3:1

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为
(3)从反应速率的角度上看,可以观察到A中反应比B中
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(5)该反应的化学方程式为
(6)反应开始至2min末,以气体X表示的平均反应速率为
(7)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是
①混合气体的压强不再变化 ②混合气体的密度不再变化 ③X的百分含量不再变化 ④混合气体的平均相对分子质量不再变化 ⑤v(X):v(Y)=3:1
| A.①②⑤ | B.①③④ | C.②③④ | D.③④⑤ |
23-24高二上·四川眉山·阶段练习
类题推荐
原电池揭示了氧化还原反应的本质是电子转移,实现了化学能转化成电能,使氧化还原反应在现代生活中获得重大应用,从而改变了人们的生活方式。
某兴趣小组为探究原电池工作原理,利用金属Zn与稀 反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作______ (填“正”或“负”)极,Zn电极上的电极反应式______ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“离子导体”中主要离子的移动方向可描述为______ 。
(3)从能量转化的角度来看,装置A中反应物的总能量______ (填“高于”、“低于”或“=”)生成物的总能量;从反应速率的角度上看,可以观察到A中反应比B中______ (填“快”或“慢”)。
(4)装置B中稀 用足量
用足量 溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为______ 。
(5)该小组同学由此得出的结论错误的是______。(多选)
某兴趣小组为探究原电池工作原理,利用金属Zn与稀

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“离子导体”中主要离子的移动方向可描述为
(3)从能量转化的角度来看,装置A中反应物的总能量
(4)装置B中稀
(5)该小组同学由此得出的结论错误的是______。(多选)
| A.任何自发进行的氧化还原反应均可以设计成原电池 |
| B.装置B中Cu电极不可用碳棒代替 |
| C.原电池的负极发生还原反应 |
| D.原电池装置中化学能全部转化为电能 |
原电池揭示了氧化还原反应的本质是电子转移,实现了化学能转化成电能,使氧化还原反应在现代生活中获得重大应用,从而改变了人们的生活方式。
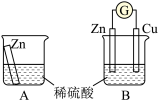
某兴趣小组为探究原电池工作原理,利用金属Zn与稀H2SO4反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作_______ (填“正”或“负”)极,Zn电极上的电极反应式为_______ ,Cu电极上的现象是_______ 。请简述确定Cu电极没有参与反应的实验依据或方案_______ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为_______ ;“离子导体”中主要离子的移动方向可描述为_______ 。
(3)从能量转化的角度来看,装置A中反应物的总能量_______ (填“高于”、“低于”或“=”)生成物的总能量;从反应速率的角度上看,可以观察到A中反应比B中_______ (填“快”或“慢”)。
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为_______ 。
(5)该小组同学由此得出的结论错误的是_______。(多选)
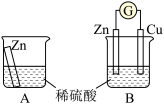
某兴趣小组为探究原电池工作原理,利用金属Zn与稀H2SO4反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为
(3)从能量转化的角度来看,装置A中反应物的总能量
(4)装置B中稀H2SO4用足量CuSO4溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
(5)该小组同学由此得出的结论错误的是_______。(多选)
| A.任何自发进行的氧化还原反应均可以设计成原电池 |
| B.装置B中Cu电极不可用碳棒代替 |
| C.原电池的负极发生还原反应 |
| D.原电池装置中化学能全部转化为电能 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网