解答题-实验探究题 适中0.65 引用1 组卷146
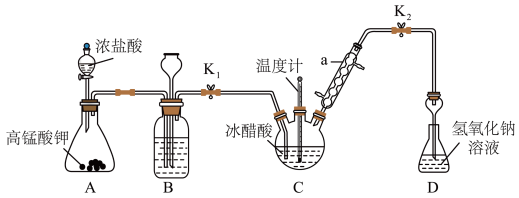
氯乙酸(ClCH2COOH)常用于制造各种染料、除锈剂等。实验室采用Cl2和CH3COOH共热法可制得氯乙酸,合成氯乙酸的装置如下图(夹持和加热装置省略)。
请回答下列问题:
(1)仪器a的名称为
___________ 。
(2)装置A中发生反应的离子方程式为
___________ 。
(3)仪器组装完成,关闭分液漏斗活塞和止水夹K2,打开K1,向装置B中长颈漏斗中注入液体至形成一段水柱,若
___________ ,则气密性良好。
(4)装置B的作用之一是观察Cl2的生成速率,则B中盛放的液体为
___________ 。实验结束时,关闭分液漏斗活塞和止水夹K1,此时装置B的作用是
___________ 。
(5)通过佛尔哈德法可以测定氯乙酸产品中氯元素的质量分数,实验步骤如下:
Ⅰ.取0.284g粗产品于锥形瓶中,加入足量NaOH溶液,煮沸,完全水解后加稀硝酸调至酸性。
Ⅱ.向锥形瓶中加入0.4200mol∙L-1的AgNO3溶液10.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2.00mL硝基苯,用力摇动,使沉淀表面被硝基苯覆盖。
Ⅳ.加入指示剂,用0.0200mol∙L-1NH4SCN标准溶液滴定过量Ag+至终点,消耗10.00mLNH4SCN溶液。
已知: ;
;

 。
。
①滴定选用的指示剂是___________ (填代号)。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是覆盖氯化银,若无此操作所测氯元素的质量分数将会___________ (填“偏大”、“偏小”或“不变”)。
③粗产品中氯元素的质量分数为___________ 。

请回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的离子方程式为
(3)仪器组装完成,关闭分液漏斗活塞和止水夹K2,打开K1,向装置B中长颈漏斗中注入液体至形成一段水柱,若
(4)装置B的作用之一是观察Cl2的生成速率,则B中盛放的液体为
(5)通过佛尔哈德法可以测定氯乙酸产品中氯元素的质量分数,实验步骤如下:
Ⅰ.取0.284g粗产品于锥形瓶中,加入足量NaOH溶液,煮沸,完全水解后加稀硝酸调至酸性。
Ⅱ.向锥形瓶中加入0.4200mol∙L-1的AgNO3溶液10.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2.00mL硝基苯,用力摇动,使沉淀表面被硝基苯覆盖。
Ⅳ.加入指示剂,用0.0200mol∙L-1NH4SCN标准溶液滴定过量Ag+至终点,消耗10.00mLNH4SCN溶液。
已知:
①滴定选用的指示剂是
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是覆盖氯化银,若无此操作所测氯元素的质量分数将会
③粗产品中氯元素的质量分数为
23-24高二上·重庆沙坪坝·阶段练习
类题推荐
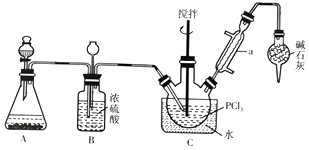
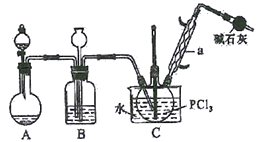
三氯氧磷(POCl3) 俗名磷酰氯、氧氯化磷,是重要的基础化工原料,可用于制取染料、农药,有机合成的氯化剂、催化剂和阻燃剂等。某化学实验小组模拟PCl3直接氧化法制备POCl3,其实验装置设计如下:
有关物质的部分性质如下表:
回答下列问题:
(1)仪器a的名称是__________ ,装置A中发生反应的化学方程式为__________________ 。
(2)B中所装试剂为__________ ,B装置的作用除观察O2的流速之外,还有_____________________ 。
(3)C装置控制反应在60℃~65℃进行,其控温的主要目的是__________ 。
(4) 实验制得的POCl3粗产品中常含有PCl3,可用__________ 方法提纯。
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液40.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖,以防止在滴加NH4SCN 时,将AgCl沉淀转化为AgSCN沉淀。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
已知: Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是__________ (填标号)。
a.FeCl2 b.甲基橙 c.淀粉 d.NH4Fe(SO4)2
②Cl元素的质量百分含量为__________ (列出算式)。
③在步骤Ⅲ中,若无加入硝基苯的操作,所测Cl-元素含量将会__________ (填“偏大”“偏小”或“不变”)。

有关物质的部分性质如下表:
| 熔点/℃ | 沸点/℃ | 其他 | |
| PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
(1)仪器a的名称是
(2)B中所装试剂为
(3)C装置控制反应在60℃~65℃进行,其控温的主要目的是
(4) 实验制得的POCl3粗产品中常含有PCl3,可用
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000mol·L-1的AgNO3溶液40.00mL,使Cl-完全沉淀。
Ⅲ.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖,以防止在滴加NH4SCN 时,将AgCl沉淀转化为AgSCN沉淀。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
已知: Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是
a.FeCl2 b.甲基橙 c.淀粉 d.NH4Fe(SO4)2
②Cl元素的质量百分含量为
③在步骤Ⅲ中,若无加入硝基苯的操作,所测Cl-元素含量将会
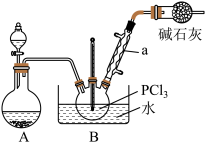
三氯氧磷( )在制药、染化、塑胶助剂等生产中有广泛应用。现设计如图实验装置(加热、夹持装置已省略)用
)在制药、染化、塑胶助剂等生产中有广泛应用。现设计如图实验装置(加热、夹持装置已省略)用 直接氧化
直接氧化 制备
制备 ,有关物质的部分性质如表:
,有关物质的部分性质如表:
回答下列问题:
(1)装置B中反应仪器的名称是___________ 。
(2)装置A中发生反应的化学方程式为___________ ;装置B中制备 的化学方程式为
的化学方程式为___________ 。
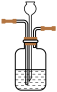
(3)该制备实验装置存在设计缺陷,改进方案为在装置A和装置B之间增加如图装置,请写出该装置的两种作用:___________ 。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素的含量,实验步骤如下:
Ⅰ、取 产品于锥形瓶中,加入足量NaOH溶液,完全反应后加稀硝酸至溶液显酸性;
产品于锥形瓶中,加入足量NaOH溶液,完全反应后加稀硝酸至溶液显酸性;
Ⅱ、向锥形瓶中加入 的
的 溶液50.00mL,使
溶液50.00mL,使 完全沉淀;
完全沉淀;
Ⅲ、向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ、加入指示剂 ,用
,用 标准溶液滴定过量
标准溶液滴定过量 至终点,记下所用体积为
至终点,记下所用体积为 。
。
已知: ,
,
①Cl元素的质量分数为___________ (列出算式即可)。
②若取消步骤Ⅲ,会使步骤Ⅳ中出现两种沉淀共存,此时
___________ ,该反应使测定结果___________ (填“偏大”“偏小”或“不变”)。

| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| -112 | 75.5 | 遇水生成 | |
| 2 | 105.3 | 遇水生成 |
(1)装置B中反应仪器的名称是
(2)装置A中发生反应的化学方程式为
(3)该制备实验装置存在设计缺陷,改进方案为在装置A和装置B之间增加如图装置,请写出该装置的两种作用:

(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素的含量,实验步骤如下:
Ⅰ、取
Ⅱ、向锥形瓶中加入
Ⅲ、向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ、加入指示剂
已知:
①Cl元素的质量分数为
②若取消步骤Ⅲ,会使步骤Ⅳ中出现两种沉淀共存,此时
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网