填空题 适中0.65 引用1 组卷145
填空
I.CO2和CH4在一定条件下合成乙酸: 完成下列填空:
完成下列填空:
(1)写出碳原子最外电子层的轨道表示式______ 。碳元素在周期表中位置:______ 。
(2)钛(Ti)是22号元素,它是______ (选填编号)。
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(3)CO2分子的电子式为______ ;其熔沸点比CS2低,原因是______ 。
Ⅱ.依据事实,写出下列反应的热化学方程式。
(4)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为______ 。
(5)根据如图写出热化学方程式______ ;
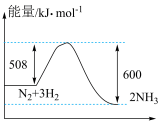
(6)已知:
且硅晶体中每个 硅原子和其他4个硅原子形成4 个共价键,工业上制取高纯硅的反应方程式为:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热为ΔH=
Si(s)+4HCl(g),该反应的反应热为ΔH=______ 。
Ⅲ.
(7)工业上常用A(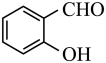 )与B(
)与B(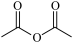 )在催化剂存在下加热反应制得香豆素(
)在催化剂存在下加热反应制得香豆素(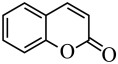 )。该反应涉及的反应类型有加成反应、
)。该反应涉及的反应类型有加成反应、______ 、______ 。
(8)写出香豆素在NaOH水溶液、加热条件下发生水解反应与化学方程式:______ 。
I.CO2和CH4在一定条件下合成乙酸:
(1)写出碳原子最外电子层的轨道表示式
(2)钛(Ti)是22号元素,它是
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(3)CO2分子的电子式为
Ⅱ.依据事实,写出下列反应的热化学方程式。
(4)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为
(5)根据如图写出热化学方程式

(6)已知:
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
Ⅲ.
(7)工业上常用A(
 )与B(
)与B( )在催化剂存在下加热反应制得香豆素(
)在催化剂存在下加热反应制得香豆素( )。该反应涉及的反应类型有加成反应、
)。该反应涉及的反应类型有加成反应、(8)写出香豆素在NaOH水溶液、加热条件下发生水解反应与化学方程式:
23-24高二上·江苏泰州·阶段练习
类题推荐
下表为元素周期表的一部分。
完成下列填空:
(1)氮原子的电子排布式为__ ,Z元素在元素周期表中的位置为__ 。
(2)上表中原子半径最大的元素是(写元素符号)__ ,该原子的核外最外层电子占有__ 个轨道。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__ 。
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1molY单质比1mol硫单质得电子多
C. Y的气态氢化物比硫的气态氢化物熔沸点高
(4)X与Z两元素的单质反应生成0.1molX的最高价化合物,恢复至室温,放热68.7 kJ,已知该化合物的溶、沸点分别为-69℃和58℃,写出该反应的热化学方程式:__ 。
(5)简述碳的同素异形体中某种单质的用途,并从晶体类型角度分析原因。___ 。
| 氮 | Y | ||
| X | 硫 | Z |
完成下列填空:
(1)氮原子的电子排布式为
(2)上表中原子半径最大的元素是(写元素符号)
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
A.Y单质与H2S溶液反应,溶液变浑浊
B.在氧化还原反应中,1molY单质比1mol硫单质得电子多
C. Y的气态氢化物比硫的气态氢化物熔沸点高
(4)X与Z两元素的单质反应生成0.1molX的最高价化合物,恢复至室温,放热68.7 kJ,已知该化合物的溶、沸点分别为-69℃和58℃,写出该反应的热化学方程式:
(5)简述碳的同素异形体中某种单质的用途,并从晶体类型角度分析原因。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
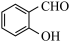 )与B(
)与B( )在催化剂存在下加热反应制得香豆素(
)在催化剂存在下加热反应制得香豆素( )。该反应涉及的反应类型有加成反应、
)。该反应涉及的反应类型有加成反应、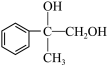 在铜催化作用下被氧气氧化的化学方程式:
在铜催化作用下被氧气氧化的化学方程式:

