解答题-原理综合题 较难0.4 引用1 组卷83
丙烯是工业上合成精细化学的原料,随着天然气和页岩气的可用性不断提高,丙烷脱氢和丙烷氧化脱氢受到了人们越来越多的关注。已知,
主反应:
副反应:

(1)相关键能的数据如下表所示:
则丙烷脱氢反应的热化学方程式为

___________  ,根据化学原理,可以同时提高化学反应速率并提高
,根据化学原理,可以同时提高化学反应速率并提高 转化率的措施是
转化率的措施是___________ 。
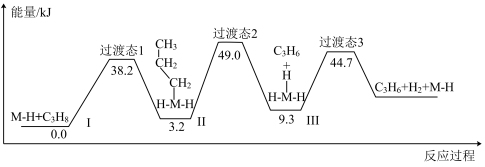
(2)用丙烷制备丙烯的机理如图所示,该反应的快慢取决于步骤___________ (填写Ⅰ、Ⅱ、Ⅲ),该反应的催化剂为___________ 。
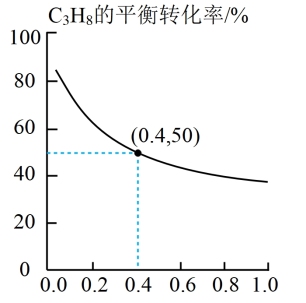
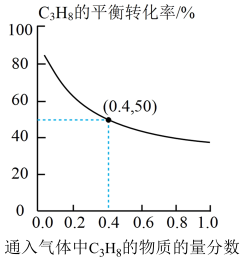
(3)在恒温条件下,向起始压强为 的恒压容器中通入
的恒压容器中通入 和
和 发生反应(
发生反应( 不参与反应)。
不参与反应)。
①下列情况能表明达到平衡状态的是___________ 。
A. 与
与 的浓度相等 B.
的浓度相等 B. 的体积分数不再改变
的体积分数不再改变
C.反应容器中压强保持不变 D.气体密度不再改变
②经过 反应达到平衡,测得
反应达到平衡,测得 的平衡转化率为50%,该条件下
的平衡转化率为50%,该条件下 的选择性为80%,则主反应的平衡常数
的选择性为80%,则主反应的平衡常数
___________ kPa(以分压表示,分压=总压×物质的量分数,保留一位小数)。
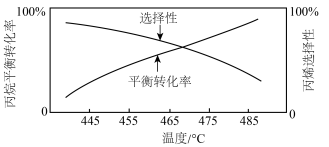
(4)已知:在纤维状 催化剂作用下,平衡时丙烷的转化率和丙烯的选择性(丙烯的选择性=
催化剂作用下,平衡时丙烷的转化率和丙烯的选择性(丙烯的选择性= ×100%)随温度的变化如图所示,丙烷的平衡转化率增大的原因是
×100%)随温度的变化如图所示,丙烷的平衡转化率增大的原因是___________ 。
主反应:
副反应:
(1)相关键能的数据如下表所示:
| 化学键 | C—C | C=C | C—H | H—H |
| 键能 | 348 | 615 | 413 | 436 |
(2)用丙烷制备丙烯的机理如图所示,该反应的快慢取决于步骤

(3)在恒温条件下,向起始压强为
①下列情况能表明达到平衡状态的是
A.
C.反应容器中压强保持不变 D.气体密度不再改变
②经过
(4)已知:在纤维状

23-24高二上·湖北黄石·阶段练习
知识点:根据△H=反应物的键能之和-生成物的键能之和进行计算活化能及其对反应速率的影响化学平衡的移动及其影响因素化学平衡常数的有关计算 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网