解答题-原理综合题 较难0.4 引用2 组卷158
(1)1883年英国化学家Claus开发了
20世纪30年代,德国法本公司将
第一阶段反应为
则第二阶段反应
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:
(3)栲胶法是我国本土自主研发和发展起来的湿法氧化脱硫方法,其原理如下(其中,TQ为醌态栲胶;THQ为酚态栲胶):
脱硫过程:
再生过程:
①基态钒原子的价电子排布式为
②根据栲胶法原理,脱硫过程中起到催化作用的物质为
(4)在密闭容器中,
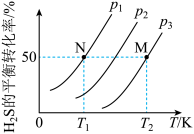
①图中压强
②初始量相同的
23-24高三上·湖北·阶段练习
类题推荐  为无色、有臭鸡蛋气味的剧毒气体,能源的开发和利用过程常伴有
为无色、有臭鸡蛋气味的剧毒气体,能源的开发和利用过程常伴有 气体生成。
气体生成。 脱硫技术是当前的重点研究方向。
脱硫技术是当前的重点研究方向。
(1)1883年英国化学家Claus开发了 氧化制硫的方法,即:
氧化制硫的方法,即:
 ,20世纪30年代,德国法本公司将
,20世纪30年代,德国法本公司将 的氧化分两阶段完成。
的氧化分两阶段完成。
第一阶段反应为
 ;
;
第二阶段反应为

_______  。
。
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:
 ,文献显示,工业上氧化锌法控制温度在
,文献显示,工业上氧化锌法控制温度在 ,请分析控制此温度区间的原因
,请分析控制此温度区间的原因_______ 。
(3)热解 制
制 。根据文献,将
。根据文献,将 和
和 的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
I

II

总反应:III
投料按体积之比 ,并用
,并用 稀释,常压,不同温度下反应相同时间后,测得
稀释,常压,不同温度下反应相同时间后,测得 和
和 体积分数如下表:
体积分数如下表:
①反应II能自发进行的条件是_______ 。
②下列说法正确的是_______ 。
A.其他条件不变时,温度越高, 的转化率越高
的转化率越高
B.断裂 键的同时断裂
键的同时断裂 键,说明反应I已达平衡状态
键,说明反应I已达平衡状态
C.恒温恒压下,增加 的体积分数,
的体积分数, 的浓度升高
的浓度升高
D.在 ,常压下,保持通入的
,常压下,保持通入的 体积分数不变,提高投料比
体积分数不变,提高投料比 ,
, 的转化率不变
的转化率不变
③在 、
、 反应条件下,只充入
反应条件下,只充入 和
和 气体进行
气体进行 热分解反应。已知反应一开始,
热分解反应。已知反应一开始, ,平衡时混合气中
,平衡时混合气中 与
与 的分压相等,则平衡常数
的分压相等,则平衡常数
_______  。[对于气相反应,用某组分
。[对于气相反应,用某组分 的平衡压强
的平衡压强 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如 ,
, 为平衡总压强,
为平衡总压强, 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(4)栲胶脱硫技术是我国独创的湿法催化氧化脱硫技术,被广泛应用于国内。栲胶脱硫技术机理如下,请在横线上补全第二步:
①
②_______ 。
③ 栲胶(醌态)
栲胶(醌态) 栲胶(酚态)
栲胶(酚态)
④栲胶(酚态) 栲胶(醌态)
栲胶(醌态)
⑤
总反应:
(1)1883年英国化学家Claus开发了
第一阶段反应为
第二阶段反应为
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:
(3)热解
I
II
总反应:III
投料按体积之比
| 温度/ | 950 | 1000 | 1050 | 1100 | 1150 |
| 0.5 | 1.5 | 3.6 | 5.5 | 8.5 | |
| 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
②下列说法正确的是
A.其他条件不变时,温度越高,
B.断裂
C.恒温恒压下,增加
D.在
③在
(4)栲胶脱硫技术是我国独创的湿法催化氧化脱硫技术,被广泛应用于国内。栲胶脱硫技术机理如下,请在横线上补全第二步:
①
②
③
④栲胶(酚态)
⑤
总反应:
云南丰富的地热能开发和利用过程中,硫磺温泉常伴有H2S气体生成。H2S为无色、有臭鸡蛋气味的剧毒气体,H2S脱硫技术是当前的重点研究方向。
(1)20世纪30年代,德国法本公司将H2S的氧化分两阶段完成。
第一阶段反应为H2S(g)+ O2(g)=SO2(g)+H2O(g) △H=-518.9kJ•mol-1,
O2(g)=SO2(g)+H2O(g) △H=-518.9kJ•mol-1,
第二阶段反应为2H2S(g)+SO2(g)=2H2O(g)+ Sx(s) △H=-96.1kJ•mol-1。
Sx(s) △H=-96.1kJ•mol-1。
19世纪英国化学家Claus开发了H2S氧化制硫的方法,即:3H2S(g)+ O2(g)=
O2(g)= Sx(s)+3H2O(g),△H=-
Sx(s)+3H2O(g),△H=-______ kJ•mol-1。
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:ZnO(s)+H2S(g) ZnS(s)+H2O(g) △H=-76.63kJ•mol-1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低
ZnS(s)+H2O(g) △H=-76.63kJ•mol-1,文献显示,工业上氧化锌法控制温度在300~400℃,分析控制此温度区间的原因:温度过低_______ ,温度过高_______ 。
(3)热解H2S制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g) 2H2(g)+S2(g) △H1=+170kJ•mol-1
2H2(g)+S2(g) △H1=+170kJ•mol-1
Ⅱ.CH4(g)+S2(g) CS2(g)+2H2(g) △H2=+64kJ•mol-1
CS2(g)+2H2(g) △H2=+64kJ•mol-1
总反应:Ⅲ.2H2S(g)+CH4(g) CS2(g)+4H2(g)
CS2(g)+4H2(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释,常压,不同温度下反应相同时间后,测得H2和CS2体积分数如表:
①反应Ⅱ能自发进行的条件是_______ 。
②恒温恒压下,增加N2的体积分数,H2的物质的量______ 。在1000℃,常压下,保持通入的H2S体积分数不变,提高投料比[c(H2S)∶c(CH4)],H2S的转化率_______ (填“增大,减小或不变”)。
③在TK、pkPa反应条件下,只充入H2S和Ar气体进行H2S热分解反应。已知反应一开始,c(H2S)∶c(Ar)=1∶3,平衡时混合气中H2S与H2的分压相等,则平衡常数Kp=_______ kPa。
(4)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg•cm-3,NA代表阿伏加德罗常数的值。氧离子的配位数为______ 。晶胞边长a为______ nm。

(1)20世纪30年代,德国法本公司将H2S的氧化分两阶段完成。
第一阶段反应为H2S(g)+
第二阶段反应为2H2S(g)+SO2(g)=2H2O(g)+
19世纪英国化学家Claus开发了H2S氧化制硫的方法,即:3H2S(g)+
(2)氧化锌法也是一种传统的脱硫方法,其反应原理如下:ZnO(s)+H2S(g)
(3)热解H2S制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g)
Ⅱ.CH4(g)+S2(g)
总反应:Ⅲ.2H2S(g)+CH4(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释,常压,不同温度下反应相同时间后,测得H2和CS2体积分数如表:
| 温度/℃ | 950 | 1000 | 1050 | 1100 | 1150 |
| H2/V(%) | 0.5 | 1.5 | 3.6 | 5.5 | 8.5 |
| CS2/V(%) | 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
②恒温恒压下,增加N2的体积分数,H2的物质的量
③在TK、pkPa反应条件下,只充入H2S和Ar气体进行H2S热分解反应。已知反应一开始,c(H2S)∶c(Ar)=1∶3,平衡时混合气中H2S与H2的分压相等,则平衡常数Kp=
(4)ZnO晶胞结构如图所示。已知:ZnO晶体的密度为ρg•cm-3,NA代表阿伏加德罗常数的值。氧离子的配位数为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网