单选题 较难0.4 引用2 组卷194
一定条件下,在体积为10L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g),反应过程如图。下列说法不正确的是
2NH3(g),反应过程如图。下列说法不正确的是


| A.t1min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间的变化关系 |
| C.0~8min,H2的平均反应速率v(H2)=0.01125mol•L-1•min-1 |
| D.10~12min,N2的平均反应速率v(N2)=0.0025mol•L-1•min-1 |
2023高三·全国·专题练习
类题推荐
向一体积为3L的恒容密闭容器中充入0.1molCH4(g)和0.2molNO2(g),在一定温度下发生反应:CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2(g),测得容器内CO2的物质的量(n)与反应时间(t)的关系如表所示。
CO2(g)+2H2O(g)+N2(g),测得容器内CO2的物质的量(n)与反应时间(t)的关系如表所示。
下列说法错误的是
| 反应时间t/min | 2 | 4 | 6 | 8 | 10 |
| CO2的物质的量n/mol | 0.04 | 0.06 | 0.07 | 0.075 | 0.075 |
| A.0~4min内,NO2的平均反应速率v(NO2)=0.1mol·L-1·min-1 |
| B.第6min时的正、逆反应速率之差大于第8min时的 |
| C.该温度下,CH4的平衡转化率为25% |
| D.第10min时,升高温度,正反应速率和逆反应速率均增大 |
一定温度和压强下,在2 L的密闭容器中合成氨气:N2(g)+3H2(g) 2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法
2NH3(g) 。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法不正确 的是:
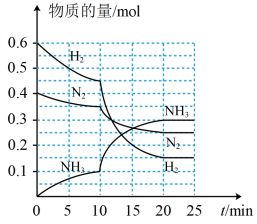

| A.0~10 min内,以NH3表示的平均反应速率为0.005 mol • L-1• min-1 |
| B.10~20 min内,NH3浓度变化的原因可能是加入催化剂 |
| C.该反应在20 min时达到化学平衡状态 |
| D.N2的平衡转化率与H2平衡转化率相等 |
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI(g)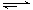 H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
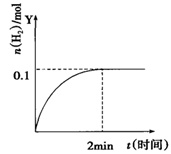
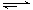 H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
| A.该温度下,反应的平衡常数是1/8 |
| B.0~2min内的HI的平均反应速率为0.05mol•L-1•min-1 |
| C.恒压下向该体系中加入N2,平衡不移动,反应速率不变 |
| D.升高温度,平衡向正反应方向移动,只有正反应速率加快 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


