单选题 适中0.65 引用1 组卷186
实验室用废CuO(含杂质FeO)制备胆矾晶体的流程如下:
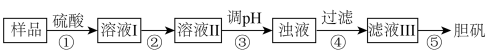
已知:pH=5时Fe3+完全水解转化为Fe(OH)3,下列分析正确的是

已知:pH=5时Fe3+完全水解转化为Fe(OH)3,下列分析正确的是
| A.用18mol/L浓硫酸配制溶解所用的4.0mol/L稀硫酸,只需3种玻璃仪器 |
| B.步骤②可向溶液Ⅰ中通入足量Cl2,将Fe2+完全转成Fe3+ |
| C.步骤③可用CuO或Cu2(OH)2CO3调节溶液的pH=5 |
| D.步骤⑤将滤液转移至蒸发皿中,加热蒸发至剩余少量液体,利用余热蒸干 |
22-23高二上·浙江嘉兴·阶段练习
类题推荐
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀),下列分析正确的是


| A.用98%的浓硫酸配制4.5 mol·L—1稀硫酸,只需3种玻璃仪器 |
| B.步骤②目的是将溶液Ⅰ中的Fe2+氧化成Fe3+,操作是通入足量的氯气 |
| C.用Cu(OH)2替代CuO也可调节溶液pH而不影响实验结果 |
| D.操作⑤是蒸发结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架 |
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀)
样品 溶液Ⅰ
溶液Ⅰ 溶液Ⅱ
溶液Ⅱ 浊液
浊液 滤液Ⅲ
滤液Ⅲ CuSO4·5H2O晶体
CuSO4·5H2O晶体
下列分析中正确的是
样品
 溶液Ⅰ
溶液Ⅰ 溶液Ⅱ
溶液Ⅱ 浊液
浊液 滤液Ⅲ
滤液Ⅲ CuSO4·5H2O晶体
CuSO4·5H2O晶体下列分析中正确的是
| A.利用Cu(OH)2替代CuO也可调节溶液pH而不影响实验结果 |
| B.步骤②目的是将溶液Ⅰ中的Fe2+充分转成Fe3+,实验操作是向溶液Ⅰ中通入足量Cl2 |
| C.用98%的浓硫酸配制溶解所用的4.5 mol·L-1的稀硫酸,只需3种玻璃仪器 |
| D.步骤④之后的实验操作是蒸干溶剂结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架 |
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀):

 ,②
,②

 →CuSO4·5H2O晶体
→CuSO4·5H2O晶体
下列分析中正确的是

 ,②
,②

 →CuSO4·5H2O晶体
→CuSO4·5H2O晶体下列分析中正确的是
| A.用98%的浓硫酸配制溶解所用的4.5 mol·L-1的稀硫酸,只需3种玻璃仪器 |
| B.步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是向溶液Ⅰ中通入足量氯气 |
| C.利用Cu(OH)2替代CuO也可调节溶液pH而不影响实验结果 |
| D.步骤④之后的实验操作是蒸干溶剂结晶,所需仪器是蒸发皿、玻璃棒、酒精灯、泥三角、三脚架 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


