解答题-原理综合题 适中0.65 引用1 组卷74
近年来我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
(1)已知:





写出 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:___________ ;并用 、
、 表示此反应的化学平衡常数
表示此反应的化学平衡常数
___________ 。
(2)为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是___________ (填字母)。
a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在250℃时,在某恒容密闭容器中进行由 催化氢化合成
催化氢化合成 的反应,如图为不同投料比[
的反应,如图为不同投料比[ ]时某反应物X的平衡转化率的变化曲线。则反应物X是
]时某反应物X的平衡转化率的变化曲线。则反应物X是___________ (填“ ”或“
”或“ ”)。
”)。
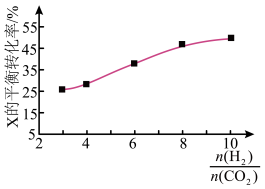
(4)在250℃时,在 的恒容密闭容器中加入
的恒容密闭容器中加入
 、
、
 及催化剂,
及催化剂, 时反应达到平衡,测得
时反应达到平衡,测得 。
。
①前 内
内 的平均反应速率
的平均反应速率
___________  。
。
②化学平衡常数
___________ (用分数表示)。
③下列描述中能说明上述反应已达平衡的是___________ (填字母)。
a.
b.单位时间内生成
 的同时生成
的同时生成

c.
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
根据上表所给数据,用 生产甲醇的最优条件为
生产甲醇的最优条件为___________ (填实验编号)。
(1)已知:
写出
(2)为提高
a.高温、高压 b.低温、低压 c.高温、低压 d.低温、高压
(3)在250℃时,在某恒容密闭容器中进行由

(4)在250℃时,在
①前
②化学平衡常数
③下列描述中能说明上述反应已达平衡的是
a.
b.单位时间内生成
c.
d.容器中气体的平均相对分子质量不随时间而变化
④催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下表四组实验数据。
| 实验编号 | 温度/K | 催化剂 | 甲醇的选择性/% | |
| A | 543 | 12.3 | 42.3 | |
| B | 543 | 11.9 | 72.7 | |
| C | 553 | 15.3 | 39.1 | |
| D | 553 | 12.0 | 70.6 |
23-24高二上·湖南湘西·阶段练习
类题推荐
我国政府明确提出2030年“碳达峰”、2060年“碳中和”目标。近年来我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究方面的力度,实现可持续发展。回答下列问题:
(1)已知:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH1=+41.1 kJ·mol-1 K1
CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.0 kJ·mol-1 K2
写出CO2催化氢化合成甲醇的热化学方程式:_______ 。用K1 、K2表示此反应的化学平衡常数K=_______ 。
(2)为提高CO2催化氢化合成甲醇的反应中CH3OH(g)的产率,理论上应采用的条件是_______(填字母)。
(3)250 ℃时,在恒容密闭容器中发生CO2(g)催化氢化合成CH3OH(g)的反应,下图为不同投料比[n(H2)/n(CO2)]时某反应物X的平衡转化率的变化曲线。反应物X是_______ (填“CO2”或“H2”)。
①前10 min内H2的平均反应速率v(H2)=_______ mol·L-1·min-1。
②化学平衡常数K=_______ 。
③下列描述中能说明上述反应已达到平衡的是_______ (填字母)。
A.3v正(H2)=v逆(CH3OH)
B.容器中气体压强不随时间而变化
C.c(H2)∶c(CO2)=1∶1
D.容器中气体的平均相对分子质量不随时间而变化
(1)已知:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH1=+41.1 kJ·mol-1 K1
CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.0 kJ·mol-1 K2
写出CO2催化氢化合成甲醇的热化学方程式:
(2)为提高CO2催化氢化合成甲醇的反应中CH3OH(g)的产率,理论上应采用的条件是_______(填字母)。
| A.高温、高压 | B.低温、低压 | C.高温、低压 | D.低温、高压 |
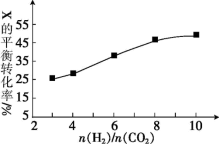
①前10 min内H2的平均反应速率v(H2)=
②化学平衡常数K=
③下列描述中能说明上述反应已达到平衡的是
A.3v正(H2)=v逆(CH3OH)
B.容器中气体压强不随时间而变化
C.c(H2)∶c(CO2)=1∶1
D.容器中气体的平均相对分子质量不随时间而变化
2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:I.CO2(g)+H2(g) H2O(g)+CO(g) △H1=+41.1kJ/mol
H2O(g)+CO(g) △H1=+41.1kJ/mol
II.CO(g)+2H2(g) CH3OH(g) △H2=-90.0kJ/mol
CH3OH(g) △H2=-90.0kJ/mol
写出CO2催化氢化合成甲醇的热化学方程式:________ 。
(2)为提高CH3OH的产率,理论上应采用的条件是________ (填选项字母)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由CO2(g)催化氢化合成 CH3OH(g),不同投料比[n(H2)/n(CO2)]时某反应物X的平衡转化率变化曲线如图所示。反应物X是_______ (填“CO2”或“H2”),判断依据是_______ 。
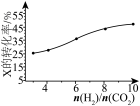
(4)250℃时,在体积为2.0 L的恒容密闭容器中加入6mol H2、2mol CO2和催化剂发生 CO2催化氢化合成甲醇的反应,10 min时反应达到平衡,测得c(CH3OH) = 0.75 mol • L-1。
①前10 min内的平均反应速率H2=_______ mol • L-1 • min-1。
②该温度下,该反应的化学平衡常数K =_______ 。
③催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下表所示:
根据上表所给数据,用CO2生产甲醇的最优选项为________ (填字母)。
(1)已知:I.CO2(g)+H2(g)
II.CO(g)+2H2(g)
写出CO2催化氢化合成甲醇的热化学方程式:
(2)为提高CH3OH的产率,理论上应采用的条件是
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由CO2(g)催化氢化合成 CH3OH(g),不同投料比[n(H2)/n(CO2)]时某反应物X的平衡转化率变化曲线如图所示。反应物X是

(4)250℃时,在体积为2.0 L的恒容密闭容器中加入6mol H2、2mol CO2和催化剂发生 CO2催化氢化合成甲醇的反应,10 min时反应达到平衡,测得c(CH3OH) = 0.75 mol • L-1。
①前10 min内的平均反应速率H2=
②该温度下,该反应的化学平衡常数K =
③催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下表所示:
| 试验编号 | 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
| C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| D | 553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
根据上表所给数据,用CO2生产甲醇的最优选项为
2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:CO2(g)+H2(g) H2O(g) +CO(g) ΔH1 =+41.1kJ/mol-1
H2O(g) +CO(g) ΔH1 =+41.1kJ/mol-1
CO(g)+2H2(g) CH3OH(g) ΔH2=-90.0kJ/mol-1
CH3OH(g) ΔH2=-90.0kJ/mol-1
写出CO2催化氢化合成甲醇的热化学方程式:__ 。
(2)为提高CH3OH转化率,理论上应采用的条件是__ (填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(3)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[ ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
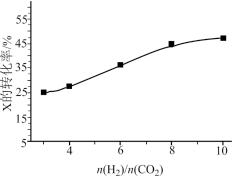
反应物X是__ (填“CO2”或“H2”),理由是___ 。
(4)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol。
①前10min的平均反应速率v(H2)=__ mol·L-1·min -1。
②化学平衡常数K=__ 。
③催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
根据上表所给数据,用CO2生产甲醇的最优选项为__ (填字母)。
(1)已知:CO2(g)+H2(g)
 H2O(g) +CO(g) ΔH1 =+41.1kJ/mol-1
H2O(g) +CO(g) ΔH1 =+41.1kJ/mol-1CO(g)+2H2(g)
 CH3OH(g) ΔH2=-90.0kJ/mol-1
CH3OH(g) ΔH2=-90.0kJ/mol-1写出CO2催化氢化合成甲醇的热化学方程式:
(2)为提高CH3OH转化率,理论上应采用的条件是
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(3)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[

反应物X是
(4)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol。
①前10min的平均反应速率v(H2)=
②化学平衡常数K=
③催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
| 实验编号 | 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
| C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| D | 553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


