单选题 适中0.65 引用2 组卷378
铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分Cu2S)可以用于制铜,反应为Cu2S +O2 2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S与浓硝酸反应可得Cu(NO3)2。Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O加入到稀硫酸中,溶液变蓝色并有紫红色固体产生。下列有关辉铜矿制备粗铜的相关说法正确的是
2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S与浓硝酸反应可得Cu(NO3)2。Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O加入到稀硫酸中,溶液变蓝色并有紫红色固体产生。下列有关辉铜矿制备粗铜的相关说法正确的是

| A.Cu+转化为基态Cu,得到的电子填充在3d轨道上 |
| B.O2和SO2都是非极性分子 |
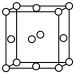
| C.Cu2S晶胞中S2-位置如图所示,则一个晶胞中含有8个Cu+ |
| D.标准状况下,每有 22.4 L O2参与反应,转移电子数为 4 mol |
23-24高三上·江苏·开学考试
类题推荐
铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分 Cu2S)可以用于制铜,反应为Cu2S +O2 2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S与浓硝酸反应可得Cu(NO3)2。Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O加入到稀硫酸中,溶液变蓝色并有紫红色固体产生,下列说法正确的是
2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S与浓硝酸反应可得Cu(NO3)2。Cu在O2存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O加入到稀硫酸中,溶液变蓝色并有紫红色固体产生,下列说法正确的是
| A.电解精炼铜时阴极反应:Cu-2e-=Cu2+ |
| B.Cu2S与浓硝酸反应Cu2S+6HNO3(浓) |
| C.Cu2O溶于稀硫酸:Cu2O+2H+=Cu+Cu2++H2O |
| D.Cu在O2 存在下与氨水反应:2Cu+8NH3+O2+4H+=2[Cu(NH3)4]2++2H2O |
铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分 Cu2S)可以用于制铜,反应为Cu2S +O2 2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S 与浓硝酸反应可得Cu(NO3)2。Cu 在O2 存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O 加入到稀硫酸中,溶液变蓝色并有紫红色固体产生。下列说法正确的是
2Cu+SO2,制得的粗铜通过电解法进行精炼。Cu2S 与浓硝酸反应可得Cu(NO3)2。Cu 在O2 存在下能与氨水反应生成[Cu(NH3)4]2+。Cu2O 加入到稀硫酸中,溶液变蓝色并有紫红色固体产生。下列说法正确的是
| A.SO2 的键角比 SO3 的大 |
| B.SO2 和 SO3 中心原子均采取 sp2 杂化 |
| C.Cu+吸引电子的能力比Cu2+的强 |
| D.1 mol [Cu(NH3)4]2+中 σ 键的数目为 12×6.02×1023 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



