解答题-实验探究题 较难0.4 引用1 组卷161
某小组设计实验探究硫酸的性质。回答下列问题:
实验(一)探究浓硫酸吸水性。如图:

实验中,向烧瓶中滴加浓硫酸,观察到烧瓶内产生大量白雾,烧杯中产生白色沉淀。
(1)烧杯中产生的白色沉淀是___________ (填化学式)。
(2)浓硫酸表现吸水性的同时还表现的性质是___________ 。
实验(二)利用稀硫酸和氢氧化钠溶液反应测定中和反应的反应热,装置如图所示:
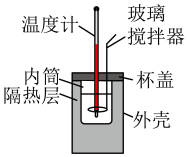
(3)实验中进行搅拌操作时应___________ ;如果用较浓硫酸替代稀硫酸进行实验,测得中和反应的反应热(△H)___________ (填“偏高”“偏低”或“无影响”)。
(4)已知25.00mL0.1 稀硫酸和50.00mL0.1
稀硫酸和50.00mL0.1 NaOH溶液恰好完全反应时,混合溶液平均温度由
NaOH溶液恰好完全反应时,混合溶液平均温度由 ℃升到
℃升到 ℃(最高),已知溶液密度近似为1
℃(最高),已知溶液密度近似为1 ,比热容为4.18
,比热容为4.18 ,生成1mol
,生成1mol (l)时的反应热为(△H)
(l)时的反应热为(△H)___________  (只列计算式)。
(只列计算式)。
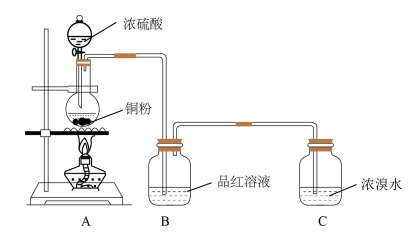
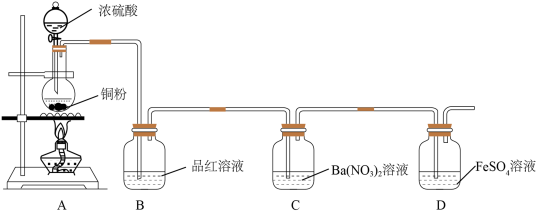
实验(三)探究浓硫酸的强氧化性。如图:
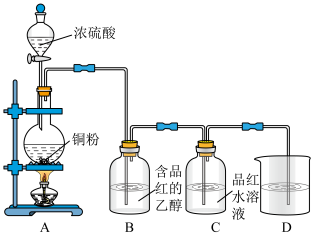
实验中发现A中有黑灰色固体,B中溶液不褪色,C中溶液褪色,实验完毕后,分离A中混合物得到黑色固体。
(5)观察A中反应产物的操作是___________ ,由上述实验证明: 漂白性本质是
漂白性本质是 与水反应,可能是
与水反应,可能是___________ (填化学式或离子符号)(填一种)与品红生成无色物质。
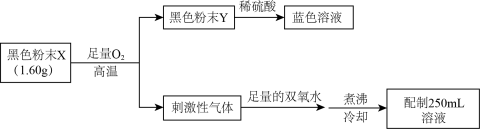
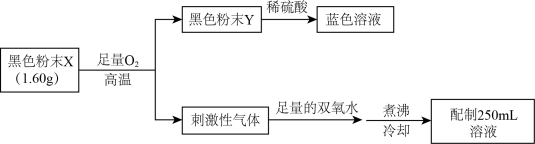
(6)经测定:纯净的黑色固体由铜、硫元素组成,为了测定其组成,取xg样品在氧气中充分灼烧,得到纯净的黑色粉末CuO,称重为yg,若x=y,则黑色固体是___________ (填化学式)。
实验(一)探究浓硫酸吸水性。如图:

实验中,向烧瓶中滴加浓硫酸,观察到烧瓶内产生大量白雾,烧杯中产生白色沉淀。
(1)烧杯中产生的白色沉淀是
(2)浓硫酸表现吸水性的同时还表现的性质是
实验(二)利用稀硫酸和氢氧化钠溶液反应测定中和反应的反应热,装置如图所示:

(3)实验中进行搅拌操作时应
(4)已知25.00mL0.1
实验(三)探究浓硫酸的强氧化性。如图:

实验中发现A中有黑灰色固体,B中溶液不褪色,C中溶液褪色,实验完毕后,分离A中混合物得到黑色固体。
(5)观察A中反应产物的操作是
(6)经测定:纯净的黑色固体由铜、硫元素组成,为了测定其组成,取xg样品在氧气中充分灼烧,得到纯净的黑色粉末CuO,称重为yg,若x=y,则黑色固体是
23-24高二上·河南·阶段练习
类题推荐
硫酸四氨合铜晶体 常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。回答下列问题:
常作杀虫剂、媒染剂。某小组设计实验制备硫酸四氨合铜晶体并测定其纯度。回答下列问题:
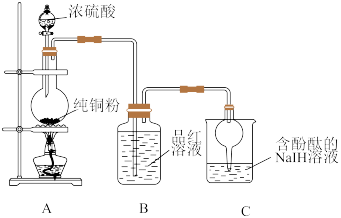
实验(一) 制备
_______ ,写出装置A中发生反应的化学方程式:_______ 。
(2)装置C中溶液由红色变为无色,体现了 具有
具有_______ (填字母)。
a.氧化性 b.还原性 c.漂白性 d.酸性氧化物的性质
(3)将装置A反应后的混合物倒入装有水的烧杯中,再加入过量的 ,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到
,充分反应后,过滤。将滤液蒸发浓缩、降温结晶、过滤,得到 晶体。
晶体。
①不能向装置A的混合物中加水,其原因是_______ 。
② 的作用是
的作用是_______ 。
实验(二)制备硫酸四氨合铜晶体
_______ (写出离子方程式)。
(5)步骤III图示装置分离晶体的突出优点有_______ (任写1条)。
实验(三)测定硫酸四氨合铜晶体的纯度
取 样品溶于蒸馏水配制成
样品溶于蒸馏水配制成 溶液,准确量取
溶液,准确量取 配制好的溶液,滴加适量的稀硫酸,充分反应。加入过量KI溶液,滴加3滴淀粉溶液,用
配制好的溶液,滴加适量的稀硫酸,充分反应。加入过量KI溶液,滴加3滴淀粉溶液,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。已知:
。已知:
 。
。
(6) 的纯度为
的纯度为_______ (用含w、c、V的代数式表示)。若振荡锥形瓶时间长,空气进入较多,则测定结果_______ (填“偏高”“偏低”或“无影响”,下同),若滴加稀硫酸过多,则测定结果_______ 。
实验(一) 制备
(2)装置C中溶液由红色变为无色,体现了
a.氧化性 b.还原性 c.漂白性 d.酸性氧化物的性质
(3)将装置A反应后的混合物倒入装有水的烧杯中,再加入过量的
①不能向装置A的混合物中加水,其原因是
②
实验(二)制备硫酸四氨合铜晶体
| 步骤 | 实验操作及主要现象 |
| A | 取一定量 |
| B | 向步骤I溶液中滴加氨水,产生蓝色沉淀;继续滴加氨水,蓝色沉淀由少到多,当达到最大后,沉淀逐渐溶解,最终得到深蓝色溶液 |
| C | 向步骤II所得溶液中加入 |
| D | 取步骤III中晶体,用乙醇与浓氨水的混合液洗涤,再用乙醇与乙醚的混合液淋洗,然后将其在60℃左右小心烘干,得到 |
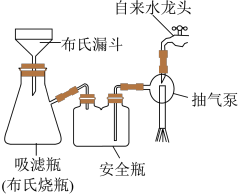
(5)步骤III图示装置分离晶体的突出优点有
实验(三)测定硫酸四氨合铜晶体的纯度
取
(6)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网