解答题-工业流程题 适中0.65 引用3 组卷193
NiOOH可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是Ni,杂质有Al、Fe、SiO2)制取NiOOH的流程如图。
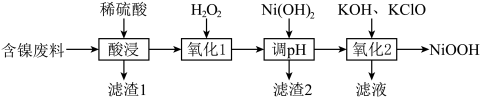
已知:ⅰ.Ni2+的性质较稳定;
ⅱ.有关金属离子沉淀的相关pH见下表
回答下列问题:
(1)Ni位于元素周期表第_______ 周期,第_______ 族。
(2)实际生产中发现H2O2的实际用量比理论用量多,原因是_______ 。
(3)“调pH”时pH的范围是_______ ,当溶液中离子浓度 时认为该离子沉淀完全,则常温下
时认为该离子沉淀完全,则常温下
_______ 。
(4)“氧化2”中反应的离子方程式为_______ 。
(5)锌镍电池是一种可充电电池,其充电时总反应为: ,则放电时正极的电极反应式为
,则放电时正极的电极反应式为_______ ,充电时阴极周围溶液pH_______ (填“增大”“减小”或“不变”)。

已知:ⅰ.Ni2+的性质较稳定;
ⅱ.有关金属离子沉淀的相关pH见下表
| 沉淀物 | ||||
| 开始沉淀时pH | 3.0 | 1.5 | 5.9 | 7.1 |
| 完全沉淀时pH | 4.7 | 3.2 | 9.0 | 9.2 |
(1)Ni位于元素周期表第
(2)实际生产中发现H2O2的实际用量比理论用量多,原因是
(3)“调pH”时pH的范围是
(4)“氧化2”中反应的离子方程式为
(5)锌镍电池是一种可充电电池,其充电时总反应为:
23-24高三上·湖北·阶段练习
类题推荐
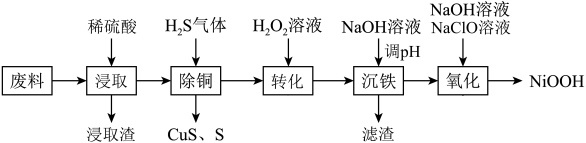
氢氧化氧镍( )难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含
)难溶于水,常用作碱性镍镉电池的电极材料。一种用含镍废料(主要含 ,以及少量
,以及少量 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如图:
的工艺流程如图: 的性质较稳定。
的性质较稳定。
回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
(2)“浸取渣”的主要成分为______ (填化学式)。
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:______ 。
(4)“转化”时 的作用是
的作用是______ ,实际生产中发现 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是______ 。
(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的 如下表所示:
如下表所示:
则“沉铁”过程中加入 溶液调节
溶液调节 的范围应为
的范围应为______ 。
(6)“氧化”时发生反应的离子方程式为______ 。若用 废料(其中
废料(其中 的质量分数为
的质量分数为 )经该流程制得
)经该流程制得 固体,则
固体,则 的产率为
的产率为______ 。( )
)
回答下列问题:
(1)为了提高“浸取”中废料的浸出效率,下列采取的措施不合理的有______(填标号)。
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.使用 |
(2)“浸取渣”的主要成分为
(3)“除铜”过程中发生了两个化学反应,写出生成S的离子方程式:
(4)“转化”时
(5)已知该工艺条件下金属阳离子生成对应氢氧化物沉淀时的
金属阳离子 | |||
开始沉淀时的pH | 1.5 | 6.5 | 7.2 |
沉淀完全时的pH | 3.2 | 9.7 | 9.2 |
(6)“氧化”时发生反应的离子方程式为
某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Fe及其他不溶于酸、碱的杂质。现用含镍废催化剂制备NiSO4·7H2O,其流程图如下:
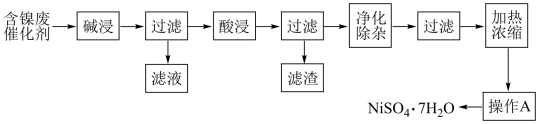
金属阳离子转化为氢氧化物沉淀的 如下表:
如下表:
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为___________ 。
(2)“酸浸”所使用的酸为___________ 。
(3)“净化除杂”时需加入H2O2溶液,写出反应的离子方程式___________ ,然后调节pH使溶液中的铁元素完全沉淀而不影响镍元素的pH范围为___________ 。
(4)“操作A”为___________ 、过滤、洗涤、干燥,即得产品。
(5)已知:NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为___________ 。

金属阳离子转化为氢氧化物沉淀的
| 金属离子 | Fe2+ | Fe3+ | Ni2+ |
| 开始沉淀 | 6.7 | 1.9 | 7.2 |
| 完全沉淀 | 9.0 | 3.2 | 9.2 |
(1)“碱浸”时发生反应的离子方程式为
(2)“酸浸”所使用的酸为
(3)“净化除杂”时需加入H2O2溶液,写出反应的离子方程式
(4)“操作A”为
(5)已知:NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为
碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS等)来制备,其工艺流程如图:

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为___ 。
(2)“溶解”时放出的气体为___ (填化学式)。
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
“调pH1”时,溶液pH范围为___ ;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式___ 。
(5)金属铬在溶液中有多种存在形式,CrO 和Cr2O
和Cr2O 在溶液中可相互转化。用离子方程式表示Na2CrO4溶液中的转化反应
在溶液中可相互转化。用离子方程式表示Na2CrO4溶液中的转化反应___ ,温度升高,溶液中CrO 的平衡转化率减小,则该反应的△H
的平衡转化率减小,则该反应的△H___ 0(填“>”、“<”或“=”)。

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为
(2)“溶解”时放出的气体为
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 开始沉淀的pH | 完全沉淀的pH | |
| Ni2+ | 6.2 | 8.6 |
| Fe2+ | 7.6 | 9.1 |
| Fe3+ | 2.3 | 3.3 |
| Cr3+ | 4.5 | 5.6 |
“调pH1”时,溶液pH范围为
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式
(5)金属铬在溶液中有多种存在形式,CrO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


