解答题-工业流程题 较难0.4 引用2 组卷838
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
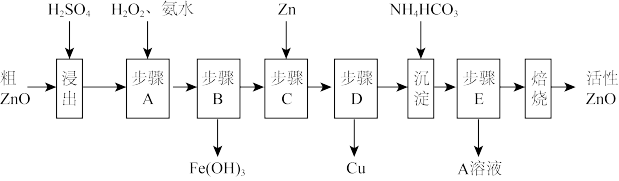
已知:几种离子生成氢氧化物沉淀时的pH如表:
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是______ ,该步骤需控制溶液pH的范围是______ 。
(2)A溶液中主要含有的溶质是______ 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS______ (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为______ mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。

已知:几种离子生成氢氧化物沉淀时的pH如表:
| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是
(2)A溶液中主要含有的溶质是
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS
(4)若经处理后的废水pH=8,此时Zn2+的浓度为
11-12高三上·江苏扬州·阶段练习
类题推荐
工业上利用粗ZnO(含FeO、CuO)制取金属锌的流程如下(部分步骤省略):
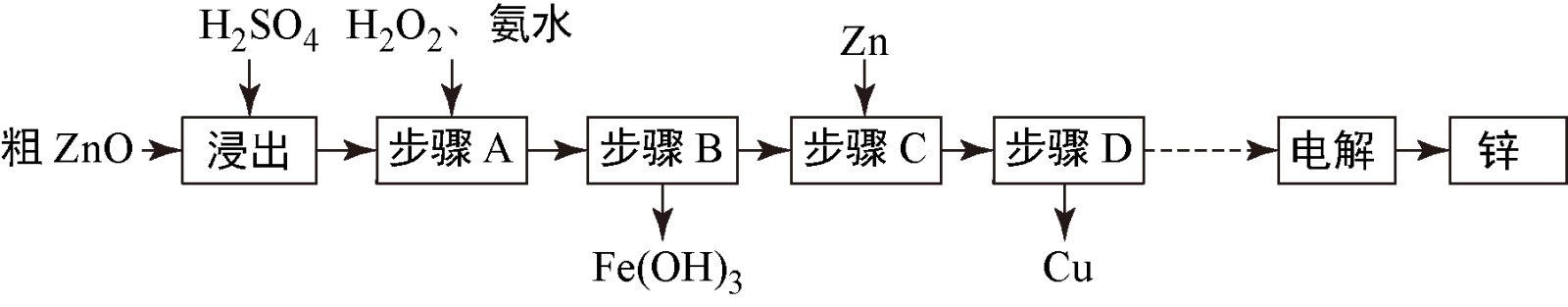
已知几种离子形成氢氧化物沉淀时的pH如下表:
请回答下列问题:
(1)酸浸粗氧化锌的过程中,为加快反应速率,可采取的措施有_______ (写一种);
(2)步骤A中,加入H2O2的目的是_______ ;加入氨水时,为了不形成Cu(OH)2、Zn(OH)2,该步骤需控制溶液pH的范围是_______ ;
(3)步骤C反应的离子方程式为_______ ;
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,则此时Fe3+的浓度为_______ ;(已知Ksp[Fe(OH)3]=4.0×10-38)

已知几种离子形成氢氧化物沉淀时的pH如下表:
| 待沉淀的离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时的pH | 6.3 | 1.5 | 6.2 | 5.2 |
| 沉淀完全时的pH | 9.7 | 3.2 | 8.0 | 6.4 |
(1)酸浸粗氧化锌的过程中,为加快反应速率,可采取的措施有
(2)步骤A中,加入H2O2的目的是
(3)步骤C反应的离子方程式为
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,则此时Fe3+的浓度为
工业上用含锌物料(含 FeO、CuO、FeS、CuS 等杂质)制取活性 ZnO 的流程如下:
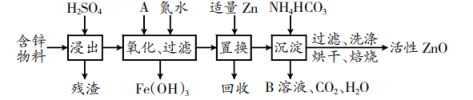
已知:各离子开始沉淀及完全沉淀时的 pH 如表所示。
(1)含锌废料中的少量 CuS 和 ZnS,加入硫酸后 ZnS 可以溶解而 CuS 不溶,则相同温度下Ksp(CuS)_______ Ksp(ZnS)(选填“>”、“<”或“=”)。
(2)第二步中先加入 A 物质的目的是_______ ,物质 A 可使用下列物质中的 _______ 。
A. O2 B. KMnO4 C. H2O2 D. Cl2
(3)加入氨水的目的是调节溶液的 pH,pH 应控制的范围是_______ 。
(4)加入 Zn 粉发生反应的离子方程式有_______ 。
(5)B 溶液溶质的化学式是_______ ,其在农业生产中的一种用途是 _______ 。

已知:各离子开始沉淀及完全沉淀时的 pH 如表所示。
| 离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 6.34 | 1.48 | 6.2 | 4.7 |
| 完全沉淀的pH | 9.7 | 3.2 | 8.0 | 6.7 |
(2)第二步中先加入 A 物质的目的是
A. O2 B. KMnO4 C. H2O2 D. Cl2
(3)加入氨水的目的是调节溶液的 pH,pH 应控制的范围是
(4)加入 Zn 粉发生反应的离子方程式有
(5)B 溶液溶质的化学式是
工业上利用粗ZnO(含FeO、CuO)制取金属锌的流程如下(部分步骤省略):
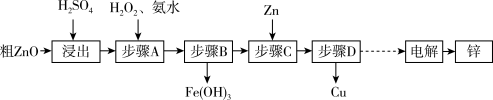
已知:几种离子形成氢氧化物沉淀时的pH如下表:
请回答下列问题:
(1)酸浸粗氧化锌的过程中,常将粗氧化锌粉碎成细颗粒,适当增加硫酸的浓度,目的是_________ 。
(2)步骤A的目的是将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2 、 Zn(OH)2 ,该步骤需控制溶液pH的范围是____________ ,该步骤中先加入H2O2充分反应后再加入氨水,写出加入H2O2的离子方程式_____________ 。
(3)步骤C的反应离子方程式为____________ 。
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,求Fe3+ 离子浓度为_________ 。(已知Ksp[Fe(OH)3]= 4.0×10-3 8)

已知:几种离子形成氢氧化物沉淀时的pH如下表:
| 待沉淀的离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 6.2 | 5.2 |
| 沉淀完全时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)酸浸粗氧化锌的过程中,常将粗氧化锌粉碎成细颗粒,适当增加硫酸的浓度,目的是
(2)步骤A的目的是将Fe2+氧化为Fe3+,并全部形成Fe(OH)3沉淀,为了暂不形成Cu(OH)2 、 Zn(OH)2 ,该步骤需控制溶液pH的范围是
(3)步骤C的反应离子方程式为
(4)若步骤A中加入H2O2后,室温下将溶液的pH调为4,求Fe3+ 离子浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


