填空题 适中0.65 引用14 组卷2132
碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
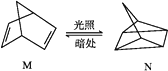
ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a________ (填“>”“<”或“=”)238.6。(已知甲醇的燃烧热为 )
)
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:____________________________ 。
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_____________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

ΔH=+88.6 kJ·mol-1,则M、N相比,较稳定的是
(2)CH3OH+O2(g) =CO2(g)+2H2O(g) ΔH=-akJ·mol-1,则a
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(4)将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) ===2Al2O3(s)+3TiC(s) ΔH= -1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
13-14高三·全国·课时练习
类题推荐
碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光照可转化成N,转化过程如下,△H= +88.6 kJ·mol-1。则M、N相比,较稳定的是_______
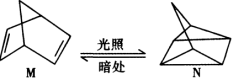
(2)已知CH3OH(l)的燃烧热为238.64 kJ∙mol−1,CH3OH(l)+O2(g)=CO2(g)+2H2(g) △H= -a kJ·mol-1,则a_______ 238.6(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s) △H=−1176kJ⋅mol−1。反应过程中每转移1mol e-放出的热量为_______ kJ。
(5)已知1mol燃料完全燃烧的数据分别为:
使用上述燃料最能体现“低碳经济”理念的是_______ 。
(1)有机物M经过太阳光照可转化成N,转化过程如下,△H= +88.6 kJ·mol-1。则M、N相比,较稳定的是

(2)已知CH3OH(l)的燃烧热为238.64 kJ∙mol−1,CH3OH(l)+O2(g)=CO2(g)+2H2(g) △H= -a kJ·mol-1,则a
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式
(4)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s) △H=−1176kJ⋅mol−1。反应过程中每转移1mol e-放出的热量为
(5)已知1mol燃料完全燃烧的数据分别为:
| 燃料 | 一氧化碳 | 甲烷 | 异辛烷(C8H18) | 乙醇 |
| △H | -283.0 kJ∙mol−1 | -891.0 kJ∙mol−1 | -5461.0 kJ∙mol−1 | -1366.8 kJ∙mol−1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

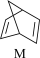
 ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1。,则M、N相比,较稳定的是

