解答题-实验探究题 适中0.65 引用1 组卷110
醋酸钠 是一种常用的防腐剂和缓冲剂。
是一种常用的防腐剂和缓冲剂。
(1)写出 水解的离子方程式
水解的离子方程式______ ,其水解平衡常数的表达式为______ 。
(2)欲用醋酸钠晶体 配制
配制 溶液,需要称量晶体的质量为
溶液,需要称量晶体的质量为______ 。实验需要的仪器有电子天平、药匙、玻璃棒、量筒、______ 。
(3)某小组探究外界因素对 水解程度的影响。
水解程度的影响。
①甲同学设计实验方案如下(表中溶液浓度均为 ):
):
i实验______ (填序号),探究加水稀释对CH3COONa水解程度的影响;
ii.实验1和3,探究加入 对CH3COONa水解程度的影响;
对CH3COONa水解程度的影响;
iii.实验1和4,探究温度对 水解程度的影响。
水解程度的影响。
②根据甲同学的实验方案,补充数据:
______ 。实验测得 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据______ (填一种微粒的化学式)的浓度增大可以说明加入 能促进
能促进 的水解。
的水解。
③已知 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是______ 。
(1)写出
(2)欲用醋酸钠晶体
(3)某小组探究外界因素对
①甲同学设计实验方案如下(表中溶液浓度均为
i实验
ii.实验1和3,探究加入
iii.实验1和4,探究温度对
序号 | 温度 | ||||
1 | 25℃ | 40.0 | 0 | 0 | |
2 | 25℃ | 4.0 | 0 | 36.0 | |
3 | 25℃ | 20.0 | 10.0 | ||
4 | 40℃ | 40.0 | 0 | 0 |
③已知
23-24高三上·上海松江·阶段练习
类题推荐
按要求回答以下问题:
(1)醋酸钠(CH3COONa)是一种常用的防腐剂和缓冲剂。某小组探究外界因素对CH3COONa水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为0.10 mol·L-1);
i.实验_______ (填序号),探究加水稀释对CH3COONa水解程度的影响;
ii.实验1和3,探究加入NH4+对CH3COONa水解程度的影响;
iii.实验1和4,探究温度对CH3COONa水解程度的影响。
①加水稀释CH3COONa溶液的过程中,下列表达式的数值变小的是_______ 。
A.c(OH-) B.c(H+)·c(OH-) C.c(H+) D.
②根据甲同学的实验方案,补充数据:a=_______ 。
③实验测得A1>A3,该结果不足以证明加入NH4+促进了CH3COONa的水解。根据_______ (填一种微粒的化学式)的浓度增大可以说明加入NH4+能促进CH3COONa的水解。
④已知CH3COONa水解为吸热反应,甲同学预测A1<A4,但实验结果为A1>A4.实验结果与预测不一致的原因是_______ 。
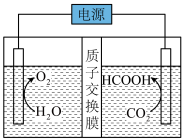
(2)温室气体CO2转化为甲酸或CO,可实现资源化利用。电还原CO2制甲酸的装置如图所示。_______ 极产生,其电极反应式为_______ 。
②理论上,该装置中每转移1mol电子,生成标准状况下的O2体积为_______ L。
(1)醋酸钠(CH3COONa)是一种常用的防腐剂和缓冲剂。某小组探究外界因素对CH3COONa水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为0.10 mol·L-1);
i.实验
ii.实验1和3,探究加入NH4+对CH3COONa水解程度的影响;
iii.实验1和4,探究温度对CH3COONa水解程度的影响。
| 序号 | 温度 | V(CH3COONa)/mL | V(CH3COONH4)/mL | V(H2O)/mL | pH |
| 1 | 25℃ | 40.0 | 0 | 0 | A1 |
| 2 | 25℃ | 4.0 | 0 | 36.0 | A2 |
| 3 | 25℃ | 20.0 | 10.0 | a | A3 |
| 4 | 40℃ | 40.0 | 0 | 0 | A4 |
A.c(OH-) B.c(H+)·c(OH-) C.c(H+) D.
②根据甲同学的实验方案,补充数据:a=
③实验测得A1>A3,该结果不足以证明加入NH4+促进了CH3COONa的水解。根据
④已知CH3COONa水解为吸热反应,甲同学预测A1<A4,但实验结果为A1>A4.实验结果与预测不一致的原因是
(2)温室气体CO2转化为甲酸或CO,可实现资源化利用。电还原CO2制甲酸的装置如图所示。
②理论上,该装置中每转移1mol电子,生成标准状况下的O2体积为
醋酸钠(CH3COONa)是一种常用的防腐剂和缓冲剂。
(1)某小组探究外界因素对CH3COONa水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为0.10 mol·L-1);
i.实验________ 和________ (填序号),探究加水稀释对CH3COONa水解程度的影响;
ii.实验1和3,探究加入 对CH3COONa水解程度的影响;
对CH3COONa水解程度的影响;
iii.实验1和4,探究温度对CH3COONa水解程度的影响。
①加水稀释CH3COONa溶液的过程中,下列表达式的数值变小的是________ 。
A.c(OH-) B.c(H+)·c(OH-) C. D.
D.
②根据甲同学的实验方案,补充数据:a=________ 。
③实验测得A1>A3,该结果不足以证明加入 促进了CH3COONa的水解。根据
促进了CH3COONa的水解。根据________ (填一种微粒的化学式)的浓度增大可以说明加入 能促进CH3COONa的水解。
能促进CH3COONa的水解。
④已知CH3COONa水解为吸热反应,甲同学预测A1<A4,但实验结果为A1>A4。实验结果与预测不一致的原因是________ 。
(2)小组通过测定不同温度下CH3COONa的水解常数Kh确定温度对CH3COONa水解程度的影响。
查阅资料:Kh= ,c0为CH3COONa溶液起始浓度。
,c0为CH3COONa溶液起始浓度。
试剂: CH3COONa溶液、0.1000 mol·L-1盐酸、pH计。
实验:测定40℃下CH3COONa水解常数Kh,完成下表中序号7的实验。
在 opiqer :fId: opiqer 50℃和60℃下重复上述实验。
数据处理:40℃下,Kh=___________ (用含V、b、c的计算式表示)
实验结论:Kh(60℃)>Kh(50℃)>Kh(40℃),温度升高,促进CH3COONa水解。
(1)某小组探究外界因素对CH3COONa水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为0.10 mol·L-1);
i.实验
ii.实验1和3,探究加入
iii.实验1和4,探究温度对CH3COONa水解程度的影响。
| 序号 | 温度 | V(CH3COONa)/mL | V(CH3COONH4)/mL | V(H2O)/mL | pH |
| 1 | 25℃ | 40.0 | 0 | 0 | A1 |
| 2 | 25℃ | 4.0 | 0 | 36.0 | A2 |
| 3 | 25℃ | 20.0 | 10.0 | a | A3 |
| 4 | 40℃ | 40.0 | 0 | 0 | A4 |
A.c(OH-) B.c(H+)·c(OH-) C.
②根据甲同学的实验方案,补充数据:a=
③实验测得A1>A3,该结果不足以证明加入
④已知CH3COONa水解为吸热反应,甲同学预测A1<A4,但实验结果为A1>A4。实验结果与预测不一致的原因是
(2)小组通过测定不同温度下CH3COONa的水解常数Kh确定温度对CH3COONa水解程度的影响。
查阅资料:Kh=
试剂: CH3COONa溶液、0.1000 mol·L-1盐酸、pH计。
实验:测定40℃下CH3COONa水解常数Kh,完成下表中序号7的实验。
| 序号 | 实验 | 记录的数据 |
| 5 | 取20.00mL CH3COONa溶液,用0.1000 mol·L-1盐酸滴定至终点,测CH3COONa溶液的浓度 | 消耗盐酸体积为V mL |
| 6 | 测40℃纯水的pH | b |
| 7 | | c |
数据处理:40℃下,Kh=
实验结论:Kh(60℃)>Kh(50℃)>Kh(40℃),温度升高,促进CH3COONa水解。
回答下列问题
(1)已知: 与
与 反应生成
反应生成 正盐的
正盐的 ;强酸、强碱的稀溶液反应的中和热的
;强酸、强碱的稀溶液反应的中和热的 。请写出
。请写出 在水溶液中电离的热化学方程式
在水溶液中电离的热化学方程式___________
(2)25℃, 的电离常数
的电离常数 为
为 ,
, 的电常数
的电常数 为
为 。
。 溶液中
溶液中
___________  (填“等于”或“小于”或“大于”)
(填“等于”或“小于”或“大于”)
(3)某小组探究外界因素对 水解程度的影响。
水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为 )
)
ⅰ.实验1和2,探究加入 对
对 水解程度的影响;
水解程度的影响;
ⅱ.实验1和3,探究温度对 水解程度的影响。
水解程度的影响。
①根据甲同学的实验方案,补充数据:a=___________ 。
②实验测得 ,该结果不足以证明加入
,该结果不足以证明加入 促进了
促进了 的水解。根据
的水解。根据___________ (填一种微粒的化学式)的浓度增大可以说明加入 能促进
能促进 的水解。
的水解。
③已知 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测 ,但实验结果为
,但实验结果为 。实验结果与预测不一致的原因是
。实验结果与预测不一致的原因是___________ 。
④小组通过测定不同温度下 的水解常数
的水解常数 确定温度对
确定温度对 水解程度的影响。
水解程度的影响。
查阅资料: ,
, 为
为 溶液起始浓度。
溶液起始浓度。
试剂: 溶液、
溶液、 盐酸、
盐酸、 计。
计。
实验:测定 水解常数
水解常数 ,完成下表中序号6的实验。
,完成下表中序号6的实验。
在 和
和 下重复上述实验。
下重复上述实验。
数据处理:用含V、b、c的计算式表示 的
的
实验结论:通过___________ ,可以说明温度升高,促进 水解。
水解。
(1)已知:
(2)25℃,
(3)某小组探究外界因素对
甲同学设计实验方案如下(表中溶液浓度均为
ⅰ.实验1和2,探究加入
ⅱ.实验1和3,探究温度对
| 序号 | 温度 | ||||
| 1 | 40.0 | 0 | 0 | ||
| 2 | 20.0 | 10.0 | a | ||
| 3 | 40.0 | 0 | 0 |
②实验测得
③已知
④小组通过测定不同温度下
查阅资料:
试剂:
实验:测定
| 序号 | 实验 | 记录的数据 |
| 4 | 取 | 消耗盐酸体积为VmL |
| 5 | 测 | b |
| 6 | c |
数据处理:用含V、b、c的计算式表示
实验结论:通过
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


