解答题-原理综合题 适中0.65 引用2 组卷223
我国力争于2030年前做到碳达峰,2060年前实现碳中和。因此,研发CO2和CH4等利用技术,降低空气中二氧化碳含量成为研究热点。
(1)N2H4(肼)常用作火箭推进剂。
已知:①
② ,
,
请写出气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O反应的热化学方程式___________ 。
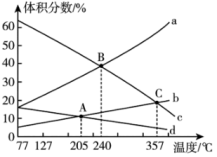
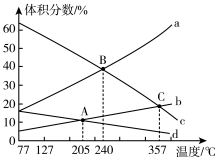
(2)TK时,向2L恒容密闭容器中充入 、
、 、
、 ,发生反应:
,发生反应: ,10min时反应达到平衡,此时CH3OH(g)的体积分数为
,10min时反应达到平衡,此时CH3OH(g)的体积分数为 ,容器内压强为pMPa。
,容器内压强为pMPa。
①0~10min内,
___________  ,平衡后,
,平衡后,
___________  ,
,
___________  (用平衡分压代替平衡浓度计算称为气体分压平衡常数,用Kp为表示,其中分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算称为气体分压平衡常数,用Kp为表示,其中分压=总压×物质的量分数)。
(1)N2H4(肼)常用作火箭推进剂。
已知:①
②
请写出气态N2H4(肼)在NO2气体中燃烧,生成N2、液态H2O反应的热化学方程式
(2)TK时,向2L恒容密闭容器中充入
①0~10min内,
22-23高二上·山东聊城·期中
类题推荐
我国力争于2060年前实现碳中和。因此,降低空气中二氧化碳含量成为研究热点,研发二氧化碳的利用技术,对于改善环境,实现绿色发展至关重要。
(1)CO2和C2H6反应制备C2H4涉及的主要反应如下:
Ⅰ.C2H6(g) C2H4(g)+H2(g) △H1=+136kJ•mol-1
C2H4(g)+H2(g) △H1=+136kJ•mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
相关的几种化学键键能如表所示:
则反应C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g)的△H3=
C2H4(g)+H2O(g)+CO(g)的△H3=______ kJ•mol-1。
(2)T℃时在2L密闭容器中通入2molC2H6和2molCO2混合气体,发生反应C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g),初始压强为mPa,反应进行到100min时达到平衡,平衡时
C2H4(g)+H2O(g)+CO(g),初始压强为mPa,反应进行到100min时达到平衡,平衡时 的体积分数为20%。0到100min内C2H6的平均反应速率为
的体积分数为20%。0到100min内C2H6的平均反应速率为______ Pa/min,则该温度下的平衡常数Kp=______ (分压=总压×物质的量分数)。
(3)乙烷热裂解制乙烯的主反应C2H6(g) C2H4(g)+H2(g),还存在副反应C2H6(g)
C2H4(g)+H2(g),还存在副反应C2H6(g) 3H2(g)+2C(s)。向乙烷热裂解制乙烯体系中加入10g的催化剂,在不同温度下,催化剂固体质量变化对催化效率的影响如图所示。
3H2(g)+2C(s)。向乙烷热裂解制乙烯体系中加入10g的催化剂,在不同温度下,催化剂固体质量变化对催化效率的影响如图所示。
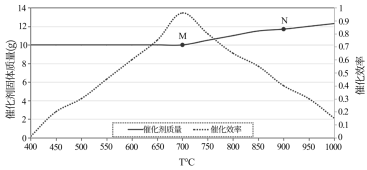
①对于主反应,图中M和N两点的化学平衡常数大小:KM______ KN(填“>”、“<”或“=”)。
②当反应温度高于700℃时催化剂固体质量增加的原因是______ 。
③当反应温度高于700℃后向体系中通入过量的CO2,可以提高催化效率的原因是______ 。
(1)CO2和C2H6反应制备C2H4涉及的主要反应如下:
Ⅰ.C2H6(g)
Ⅱ.CO2(g)+H2(g)
相关的几种化学键键能如表所示:
| 化学键 | C=O | H—H | C≡O | H—O |
| 键能/(kJ•mol-1) | 803 | 436 | 1072 | 464.5 |
(2)T℃时在2L密闭容器中通入2molC2H6和2molCO2混合气体,发生反应C2H6(g)+CO2(g)
(3)乙烷热裂解制乙烯的主反应C2H6(g)

①对于主反应,图中M和N两点的化学平衡常数大小:KM
②当反应温度高于700℃时催化剂固体质量增加的原因是
③当反应温度高于700℃后向体系中通入过量的CO2,可以提高催化效率的原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网