解答题-实验探究题 较难0.4 引用1 组卷141
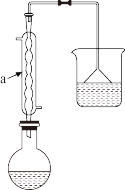
1-溴丁烷可作稀有元素萃取剂、烃化剂及有机合成的原料。实验室合成1-溴丁烷的装置(加热及夹持装置略去)及有关数据如下:

发生的反应如下:


实验步骤如下:
①在圆底烧瓶中加入14mL水,再慢慢分批加入19mL(0.54mol)浓硫酸,混合均匀并冷却至室温后,再依次加入12mL1-丁醇(0.13mol)和16.5g(0.16mol)溴化钠,充分振荡后加入2粒沸石。加热至沸,调整加热速度,以保持沸腾而又平稳回流,并不时摇动烧瓶促使反应完成。回流约30min。
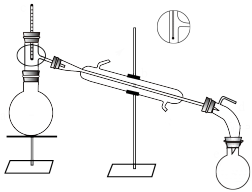
②待反应液冷却后,改回流装置为蒸馏装置,蒸出粗产物。将馏出液移至分液漏斗中,加入10mL的水洗涤,静置分层后,将产物转入另一干燥的分液漏斗中,用8mL的浓硫酸洗涤,分去硫酸层后有机相依次用10mL的水、饱和碳酸氢钠溶液和水洗涤后,转入干燥的锥形瓶中,加入1~2g的无水氯化钙干燥,间歇摇动锥形瓶,直到液体清亮为止。将过滤后的产物移至小蒸馏瓶中,蒸馏,收集99~103℃的馏分,得到产物12.0g。
回答下列问题:
(1)实验时需小火加热,若大火加热,有机相显红棕色,因为生成了___________ (填化学式),可在后处理时用少量亚硫酸氢钠水溶液洗涤以除去,发生的离子反应方程式为___________ 。
(2)实验中1-丁醇会发生其它副反应,生成的有机副产物结构简式为___________ (任写一种)。
(3)粗蒸馏 终点的判断:1-溴丁烷是否蒸馏完全,可以从下列哪些方面判断___________?
(4)用浓硫酸洗涤粗产品后,有机相应从分液漏斗___________ (填“上口倒出”或“下口放出”)。
(5)用饱和的碳酸氢钠溶液洗涤前先要用水洗一次的原因是___________ 。
(6)加入氯化钙干燥后要滤除干燥剂再蒸馏,若不滤除会产生的影响是___________ 。
(7)本实验中1-溴丁烷的产率为___________ (保留两位有效数字)。

| 名称 | 分子量 | 性状 | 密度g/mL | 熔点 | 熔点 | 溶解度g/100mL溶剂 | ||
| 水 | 醇 | 醚 | ||||||
| 1-丁醇 | 74.0 | 无色透明液体 | 0.802 | 117.7 | 7.920 | |||
| 1-溴丁烷 | 137.0 | 无色透明液体 | 1.299 | 101.6 | 不溶 | |||
实验步骤如下:
①在圆底烧瓶中加入14mL水,再慢慢分批加入19mL(0.54mol)浓硫酸,混合均匀并冷却至室温后,再依次加入12mL1-丁醇(0.13mol)和16.5g(0.16mol)溴化钠,充分振荡后加入2粒沸石。加热至沸,调整加热速度,以保持沸腾而又平稳回流,并不时摇动烧瓶促使反应完成。回流约30min。
②待反应液冷却后,改回流装置为蒸馏装置,蒸出粗产物。将馏出液移至分液漏斗中,加入10mL的水洗涤,静置分层后,将产物转入另一干燥的分液漏斗中,用8mL的浓硫酸洗涤,分去硫酸层后有机相依次用10mL的水、饱和碳酸氢钠溶液和水洗涤后,转入干燥的锥形瓶中,加入1~2g的无水氯化钙干燥,间歇摇动锥形瓶,直到液体清亮为止。将过滤后的产物移至小蒸馏瓶中,蒸馏,收集99~103℃的馏分,得到产物12.0g。
回答下列问题:
(1)实验时需小火加热,若大火加热,有机相显红棕色,因为生成了
(2)实验中1-丁醇会发生其它副反应,生成的有机副产物结构简式为
(3)
| A.看是否有馏出液,若没有,说明蒸馏已达终点 |
| B.看蒸馏烧瓶中油层是否完全消失,若完全消失,说明蒸馏已达终点 |
| C.取一试管收集几滴馏出液,加水摇动观察无油珠出现。如无,表示馏出液中已无有机物、蒸馏完成 |
| D.取一试管收集几滴馏出液,加硝酸银溶液,如无淡黄色沉淀生成表示馏出液中已无有机物、蒸馏完成 |
(5)用饱和的碳酸氢钠溶液洗涤前先要用水洗一次的原因是
(6)加入氯化钙干燥后要滤除干燥剂再蒸馏,若不滤除会产生的影响是
(7)本实验中1-溴丁烷的产率为
23-24高三上·四川成都·开学考试
类题推荐
1-溴丁烷常用作稀有元素萃取剂、烃化剂及合成染料和香料的有机原料。实验室制备1-溴丁烷的反应、主要装置和有关数据如下:NaBr+H2SO4 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
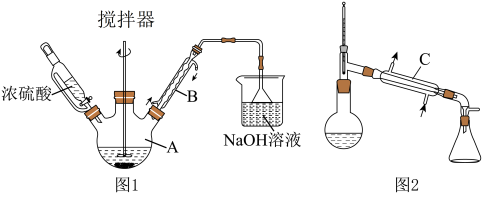
实验步骤:
在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。
将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是___________ 。仪器B与仪器C___________ (填“能”或“不能”)交换使用。
(2)NaOH溶液的作用是___________ 。
(3)粗品经第一次水洗后,所得产物略带红棕色,其原因是___________ 。
用浓硫酸洗涤的主要目的是___________ ,在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的___________ (填“上口倒出”或“下口放出”)。
(4)产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠溶液洗涤而先用水洗,其原因是___________ 。
(5)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式___________ 。
(6)本实验中,1-溴丁烷的产率为___________ (保留三位有效数字)。

| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g/cm3) | 溶解性 | |
| 正丁醇 | 74 | -89.8 | 117.7 | 0.81 | 微溶于水,易溶于浓硫酸和有机溶剂 |
| 1-溴丁烷 | 137 | -112.4 | 101.6 | 1.28 | 不溶于水,易溶于醇、醚等有机溶剂 |
| 浓硫酸 | 98 | 10.3 | 338 | 1.84 | 易溶于水 |
在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。
将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是
(2)NaOH溶液的作用是
(3)粗品经第一次水洗后,所得产物略带红棕色,其原因是
用浓硫酸洗涤的主要目的是
(4)产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠溶液洗涤而先用水洗,其原因是
(5)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式
(6)本实验中,1-溴丁烷的产率为
1-溴丁烷常用作稀有元素萃取剂、烃化剂及合成染料和香料的有机原料。实验室制备1-溴丁烷的反应、主要装置和有关数据如下:
NaBr+H2SO4 NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr
NaHSO4+HBr↑、CH3CH2CH2CH2OH+HBr CH3CH2CH2CH2Br+H2O。
CH3CH2CH2CH2Br+H2O。
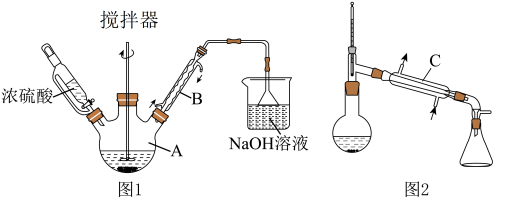
实验步骤:在仪器A中加入10mL水,边搅拌边缓慢滴加20mL过量的浓硫酸,冷却至室温。再依次加入7.4g正丁醇、16.5g研细的溴化钠和几粒沸石。在不断搅拌下,用图1所示装置小火加热回流90min,得到粗品。将粗品依次用15mL水、7mL浓硫酸、10mL水、10mL饱和碳酸氢钠溶液、10mL水洗涤并分液,分出的产物用无水氯化钙充分干燥,滤除氯化钙固体,用图2所示装置加热蒸馏,收集99~103℃的馏分,得纯净1-溴丁烷9.3g。
回答下列问题:
(1)仪器B的名称是___________ 。仪器B与仪器C___________ (填“能”或“不能”)交换使用。
(2)在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的___________ (填“上口倒出”或“下口放出”)。
(3)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式___________ 。
(4)本实验中,1-溴丁烷的产率为___________ (保留三位有效数字)。
NaBr+H2SO4

| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度(g/cm3) | 溶解性 | |
| 正丁醇 | 74 | -89.8 | 117.7 | 0.81 | 微溶于水,易溶于浓 硫酸和有机溶剂 |
| 1-溴丁烷 | 137 | -112.4 | 101.6 | 1.28 | 不溶于水,易溶于醇、 醚等有机溶剂 |
| 浓硫酸 | 98 | 10.3 | 338 | 1.84 | 易溶于水 |
回答下列问题:
(1)仪器B的名称是
(2)在用浓硫酸洗涤、分液的操作中,待液体分层后,产物应从分液漏斗的
(3)本实验最可能产生两种有机副产物,任写其中一种副产物的结构简式
(4)本实验中,1-溴丁烷的产率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网