填空题 较易0.85 引用2 组卷643
研究化学反应的快慢和限度,对工农业生产和人们生活有重要的意义。
Ⅰ.某化学课外小组的同学通过铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
(注:气体体积均在相同条件下测得)
(1)实验①和②探究盐酸浓度对反应速率的影响,即V1为_______ mL;实验②和③表明_______ 对反应速率的影响。
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是_______ 。(用文字表达)
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是_______ ;后期速率慢慢减小的主要原因是_______ 。
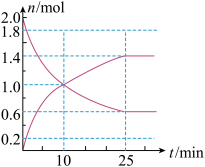
Ⅱ.工业制硫酸的反应之一为:2SO2(g)+O2(g) 2SO3(g),在1L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。
2SO3(g),在1L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。_______ ;平衡时SO2的转化率为_______ 。
(5)下列叙述不能 判断该反应达到平衡状态的是_______ ;
a.容器中压强不再改变
b.容器中气体密度不再改变
c.O2的物质的量浓度不再改变
d.SO3的质量不再改变
e.2V正(SO2)=V逆(O2)
Ⅰ.某化学课外小组的同学通过铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
| 序号 | 反应温度/℃ | V(H2O)/mL | 10gFe的形状 | t/min | ||
| ① | 20 | 2 | 5 | V1 | 块状 | 1 |
| ② | 20 | 2 | 10 | 0 | 块状 | 1 |
| ③ | 20 | 2 | 10 | 0 | 粉末 | 1 |
| ④ | 40 | 2 | 10 | 0 | 块状 | 1 |
(1)实验①和②探究盐酸浓度对反应速率的影响,即V1为
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是
Ⅱ.工业制硫酸的反应之一为:2SO2(g)+O2(g)
(5)下列叙述
a.容器中压强不再改变
b.容器中气体密度不再改变
c.O2的物质的量浓度不再改变
d.SO3的质量不再改变
e.2V正(SO2)=V逆(O2)
22-23高一下·广东东莞·期中
类题推荐
某化学课外小组的同学通过实验探究化学反应速率和化学反应限度。
I.通过铁和稀硫酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:(气体体积均在相同条件下测得)
(1)实验①和②表明,_______ 对反应速率有影响;实验①和③表明,_______ 对反应速率有影响。
(2)实验室制氢气时,可在锌和稀硫酸反应的容器中加入少量硫酸铜固体以加快反应速率,原因是_______ 。(用文字表达)
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始时速率慢慢增大,后来慢慢减小。开始时速率慢慢增大的主要原因是_______ ;后来速率慢慢减小的主要原因是_______ 。
II.在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示。
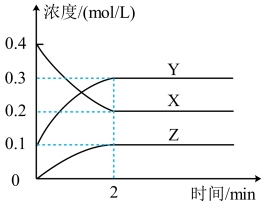
(4)该反应的化学方程式为_______ ,0~2min内的化学反应速率v(X)=_______ 。
I.通过铁和稀硫酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:(气体体积均在相同条件下测得)
| 序号 | 反应温度/℃ | 10g Fe的形状 | t/min | ||
| ① | 20 | 2 | 10 | 块状 | 1 |
| ② | 20 | 4 | 10 | 块状 | 1 |
| ③ | 20 | 2 | 10 | 粉末 | 1 |
| ④ | 40 | 2 | 10 | 粉末 | 1 |
| ⑤ | 40 | 4 | 10 | 粉末 | 1 |
(2)实验室制氢气时,可在锌和稀硫酸反应的容器中加入少量硫酸铜固体以加快反应速率,原因是
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始时速率慢慢增大,后来慢慢减小。开始时速率慢慢增大的主要原因是
II.在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示。

(4)该反应的化学方程式为
某化学课外小组的同学通过实验探究化学反应速率和化学反应限度。
I.通过铁和稀硫酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:(气体体积均在相同条件下测得)
(1)实验①和②表明,___________ 对反应速率有影响;实验①和③表明,___________ 对反应速率有影响。
(2)实验室制氢气时,可在锌和稀硫酸反应的容器中加入少量硫酸铜固体以加快反应速率,原因是___________ 。(用文字表达)
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始时速率慢慢增大,后来慢慢减小。开始时速率慢慢增大的主要原因是___________ ;后来速率慢慢减小的主要原因是___________ 。
II.在300℃时, 三种气体在恒容密闭容器中反应时的浓度变化如图所示。
三种气体在恒容密闭容器中反应时的浓度变化如图所示。
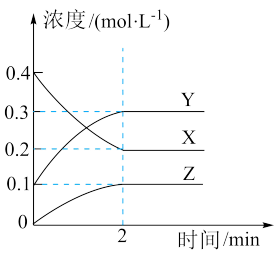
(4)该反应的化学方程式为___________ , 内的化学反应速率
内的化学反应速率
___________
(5)平衡时,Y的体积分数为___________ ;下列事实能表明300℃时该反应处于平衡状态的是___________ (填标号)。
A.容器内气体压强保持不变
B.生成Y、Z的速率之比为2:1
C.气体的密度保持不变
D.
I.通过铁和稀硫酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:(气体体积均在相同条件下测得)
| 序号 | 反应温度/℃ | ||||
| ① | 20 | 2 | 10 | 块状 | 1 |
| ② | 20 | 4 | 10 | 块状 | 1 |
| ③ | 20 | 2 | 10 | 粉末 | 1 |
| ④ | 40 | 2 | 10 | 粉末 | 1 |
| ⑤ | 40 | 4 | 10 | 粉末 | 1 |
(1)实验①和②表明,
(2)实验室制氢气时,可在锌和稀硫酸反应的容器中加入少量硫酸铜固体以加快反应速率,原因是
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始时速率慢慢增大,后来慢慢减小。开始时速率慢慢增大的主要原因是
II.在300℃时,

(4)该反应的化学方程式为
(5)平衡时,Y的体积分数为
A.容器内气体压强保持不变
B.生成Y、Z的速率之比为2:1
C.气体的密度保持不变
D.
某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度,通过实验室制备铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
(注:气体体积均在相同条件下测得)
(1)实验①和②表明,___________ 对反应速率有影响:实验①和③表明___________ 对反应速率的影响。
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是___________ 。(用文字表达)
(3)若四组实验均反应进行1分钟(铁有剩余),则以上实验需要测出的数据是___________ 。
(4)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是___________ ; 后期速率慢慢减小的主要原因是___________ 。
(5)写出铁与稀盐酸反应的离子方程式___________ 。
| 序号 | 反应温度/℃ | 10gFe的形状 | t/min | ||
| ① | 20 | 2 | 10 | 块状 | 1 |
| ② | 20 | 4 | 10 | 块状 | 1 |
| ③ | 20 | 2 | 10 | 粉末 | 1 |
| ④ | 40 | 2 | 10 | 粉末 | 1 |
| ⑤ | 40 | 4 | 10 | 粉末 | 1 |
(1)实验①和②表明,
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是
(3)若四组实验均反应进行1分钟(铁有剩余),则以上实验需要测出的数据是
(4)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是
(5)写出铁与稀盐酸反应的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


